
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 合成纤维和光导纤维都是新型有机非金属材料 | |
| C. | “玉不琢不成器”、“百炼方能成钢”发生的均为化学变化 | |
| D. | “火树银花”中的焰火实质上是金属元素的焰色反应 |
分析 A.油脂的相对分子质量较小,不属于高分子化合物;
B.光导纤维的主要成分为二氧化硅,为无机非金属材料;
C.“玉不琢不成器”只是玉的形状改变;
D.焰色反应为某些金属元素的性质.
解答 解:A.淀粉、纤维素属于天然高分子化合物,而油脂不属于高分子化合物,故A错误;
B.合成纤维是有机非金属材料,光导纤维是新型无机非金属材料,故B错误;
C.“玉不琢不成器”只是玉的形状改变,为物理变化,故C错误;
D.焰色反应为元素的性质,则节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩,故D正确;
故选D.
点评 本题考查物质组成、结构和性质的关系,题目难度不大,明确常见元素及其化合物组成、性质及用途为解答关键,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,15g甲基(-CH3)所含的中子数为6NA | |
| B. | a gO2和O3的混合气体中含有的分子总数为$\frac{a{N}_{A}}{32}$ | |
| C. | 在1L的碳酸钠溶液中,若c(CO32-)=1mol•L-1,则Na+个数为2NA | |
| D. | 78g过氧化钠晶体中,含2NA个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氧气反应时特移电子数为2NA | |
| B. | 1molCnH2n+2(n≥2)中含有的C-C键数为(n-1)NA | |
| C. | 0.1mol24Mg32S晶体中所含中子总数为28NA | |
| D. | 标准状况下,11.2LSO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
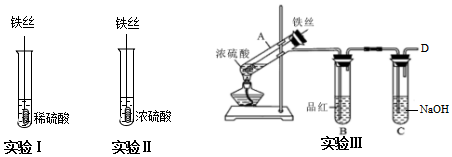
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
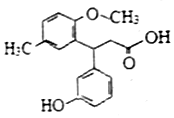
| A. | 所有碳原子可以共平面 | B. | 分子中有1个手性碳原子 | ||
| C. | 能与Na2CO3溶液反应 | D. | 能发生加成、取代、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com