
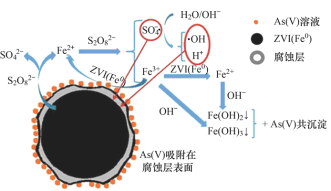
【题目】《环境科学》刊发了我国采用零价铁活化过硫酸钠(Na2S2O8,其中S为+6价)去除废水中的+5价砷[As(V)]的科研成果,反应机理如图。设NA为阿伏加德罗常数的值,Ksp[Fe(OH)3]=2.7×10-39。下列叙述正确的是
A.1mol过硫酸钠(Na2S2O8)含2NA个过氧键
B.若56gFe参加反应,共有1.5NA个S2O82-被还原
C.碱性条件下,硫酸根自由基发生反应的方程式为:SO4-·+ OH- =SO42- +·OH
D.室温下,pH越大,越有利于去除废水中的+5价砷,溶液中c(Fe3+)为2.7×10-27mol·L-1
【答案】BC
【解析】
A. 过硫酸钠(Na2S2O8)中S为+6价,Na为+1价,假设含有x个O2,含有y个O22,则x + 2y = 8,(+1) ×2+ (+6) ×2 + ( 2)×x+( 2)×y =0,则x =6,y=1,因此1mol过硫酸钠(Na2S2O8)含NA个过氧键,故A错误;
B. 若56gFe参加反应即1mol,1mol Fe先和S2O82变为1mol Fe2+,根据A选项的1mol过硫酸钠(Na2S2O8)含1mol过氧键,再根据得失电子守恒消耗1mol S2O82,接着是1molFe2+与S2O82反应生成1molFe3+,根据得失电子守恒消耗0.5mol S2O82,因此总共消耗1.5mol S2O82,即共有1.5NA个S2O82被还原,故B正确;
C. 碱性条件下,根据反应机理,硫酸根自由基发生反应的方程式为:SO4-·+ OH-=SO42 +·OH,故C正确;
D. 室温下,pH越大,亚铁和铁离子变为氢氧化亚铁和氢氧化铁,越有利于去除废水中的+5价砷,Fe(OH)3溶于水存在沉淀溶解平衡:Fe(OH)3(s) ![]() Fe3+ (aq) + 3OH-(aq),此溶液碱性极弱,pH接近7,即c(OH-) = 1×107mol·L1,因为
Fe3+ (aq) + 3OH-(aq),此溶液碱性极弱,pH接近7,即c(OH-) = 1×107mol·L1,因为![]() ,则
,则![]()
![]() ,故D错误。
,故D错误。
综上所述,答案为BC。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铁在史前就为人们所知,由于铁、钴、镍性质很相似故称为铁系元素。回答下列问题:
(1)铁、钴、镍中未成对电子数目最多的为_____,镍的外围电子轨道表达式为_____。
(2)Co2+可以和SCN-作用形成蓝色配离子,该反应可用于Co2+的定性检验。
①SCN-的空间构型为____,组成元素中第一电离能最大的是___。
②SCN-对应的酸有硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中后者沸点较高,主要原因是_________________。
(3)二茂铁是一种夹心式结构的配合物,通常认为是由一个Fe2+离子和两个C5H5-离子形成的,X射线研究结果指出两个C5H5-环的平面是平行的,结构如图1所示。C5H5-中碳原子的杂化类型为_____。分子中的大π键盘可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键盘电子数,则C5H5-中的大π键盘可以表示为______。
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键盘电子数,则C5H5-中的大π键盘可以表示为______。
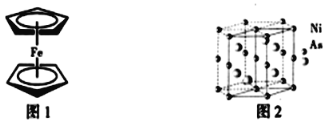
(4)NiAs晶体中的原子堆积方式如图2所示,其中As的配位数为______。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,NiAs的密度为______g·cm-3,(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,等体积、PH相同的盐酸和醋酸溶液分别加水稀释,溶液中的随溶液体积变化的曲线如图所示。据图判断下列说法正确的是

A.b点酸的总浓度大于a点酸的总浓度
B.b点溶液的导电性比c点溶液的导电性弱
C.取等体积的a点、b点对应的溶液,消耗的NaOH的量相同
D.曲线Ⅰ表示的是盐酸的变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.c(Fe3+)=0.1 mol·L-1的溶液中:Na+、Cu2+、Cl-、SCN-
B.使甲基橙变红色的溶液中:K+、Fe2+、Cl-、MnO4-
C.由水电离出的c(H+)=10-12mol·L-1的溶液:Na+、K+、CO32-、SO42-
D.![]() =10-12的溶液中:Mg2+、Al3+、NO3-、SO42-
=10-12的溶液中:Mg2+、Al3+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中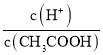 减小
减小
B.CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向0.1 mol·L-1氨水中加入少量硫酸铵固体,溶液中![]() 增大
增大
D.向AgCl、AgBr的饱和溶液中加入少量硝酸银,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3,FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
(1)用FeO作载氧剂,部分反应的lgKp与温度的关系如图所示。[已知:平衡常数Kp是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]

①图中涉及的反应中,属于吸热反应的是反应_________________(填字母)。
②R点对应温度下,向某恒容密闭容器中通入1.5 mol CO,并加入足量的FeO,只发生反应CO(g)+ FeO(s) ![]() CO2(g) +Fe(s),则CO的平衡转化率为______________
CO2(g) +Fe(s),则CO的平衡转化率为______________
(2)在T℃下,向某恒容密闭容器中加入2 mol CH4(g)和8 mol FeO(s)进行反应:CH4(g)+4FeO(s) ![]() 4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为P0,达到平衡状态时,容器的气体压强是起始压强的2倍。
4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为P0,达到平衡状态时,容器的气体压强是起始压强的2倍。
①T℃下,该反应的Kp = ______________
②若起始时向该容器中加入1molCH4(g),4molFeO(s),1mol H2O(g),0.5molCO2(g),此时反应向__________________(填“正反应”或“逆反应”)方向进行。
③其他条件不变,若将该容器改为恒压密闭容器,则此时CH4的平衡转化率___________(填“增大” “减小”或“不变”)。
(3)一种微胶囊吸收剂,将煤燃烧排放的CO2以安全、高效的方式处理掉,胶囊内部充有Na2CO3溶液,其原理如图所示。
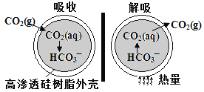
①这种微胶囊吸收CO2的原理是___________________(用离子方程式表示)。
②在吸收过程中当n(CO2):n(Na2CO3)=1:3时,溶液中c(CO32-)_____c(HCO3-)(填“>”、“ <”或“=”)
③将解吸后的CO2催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) △H1= -1323kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H2= -483.6kJ·mol-1
2CO2(g)+6H2(g)=C2H4(g)+4H2O(g) △H3=_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业冶炼钛的第一步反应为:TiO2(s)+2C(s)+2Cl2![]() TiCl4(g)+2CO。下列关于该反应的说法正确的是( )
TiCl4(g)+2CO。下列关于该反应的说法正确的是( )
A.TiCl4既是氧化产物又是还原产物
B.氧化剂与还原剂的物质的量之比为1:1
C.当转移电子数目为0.2NA时,气体体积增大1.12L
D.当有26g固体参加反应时,转移电子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以干海带为原料提取碘单质和氯化钾的过程主要分三步:完成下列填空:
(1)步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在_____________(填写仪器名称)中加热,选用热水而不是冷水浸泡海带灰的目的是____。
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I-,制得富碘溶液。实验室模拟氧化过程的实验装置如图所示。
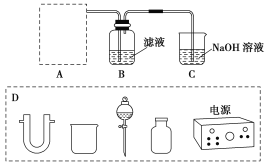
装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl-;二是电解法。限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是________(选填编号)。
a.2NaCl(s)+MnO2+2H2SO4(浓)加热MnSO4+Cl2↑+Na2SO4+2H2O
b.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O通电2NaOH+Cl2↑+H2↑
d.4HCl(浓)+MnO2加热MnCl2+Cl2↑+2H2O
广口瓶B中发生反应的离子方程式是____________。装置C中NaOH的作用是_______________。
(3)步骤三:取100 mL B中富碘溶液,按如下流程分离碘单质。
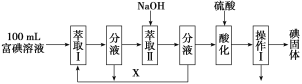
萃取Ⅱ和酸化过程发生的反应分别是:
3I2+6OH-→5I-+IO3-+3H2O;
5I-+IO3-+6H+→3I2+3H2O;
萃取剂X应选择________(选填编号)。
a.100 mL苯 b.10 mL乙醇 c.10 mL CCl4 d.10 mL己烯
实验室进行萃取操作的仪器是________。操作Ⅰ的名称是________。
(4)分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:①要用到的化学试剂是_________(填写化学式);②要测定的物理量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出或完成下列热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式__________。
(2)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
化学键 | C-H | C-F | H-F | F-F |
键能kJ/mol | 414 | 489 | 565 | 155 |
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为_____。
(3)1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:______。
(4)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为__________;
②氢气燃烧热的热化学方程式为________;
(5)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=_______kJ·mol-1;
(6)白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH为_____。
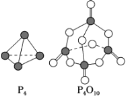
(7)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
相同状况下,能量较低的是________;白磷的稳定性比红磷________(填“大”或“小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com