
| A. | Na3PO4 | B. | Na3PO3 | ||
| C. | Na4P2O7 和Na5P3O10 | D. | Na3PO4、Na4P2O7和Na5P3O10 |
分析 48gNaOH的物质的量为1.2mol,58.8g固态纯H3PO4的物质的量为0.6mol,得到79.8g固体A和27g水,反应物总质量等于生成物总质量,说明钠与磷全部转化到A中,生成水的物质的量为1.5mol,根据H元素守恒可知,A中没有H元素,含有氧元素为0.6mol×4+1.2mol-1.5mol=2.1mol,结合原子数目之比判断.
解答 解:48gNaOH的物质的量为$\frac{48g}{40g/mol}$=1.2mol,58.8g固态纯H3PO4的物质的量为$\frac{58.8g}{98g/mol}$=0.6mol,得到79.8g固体A和27g水,反应物总质量等于生成物总质量,说明钠与磷全部转化到A中,生成水的物质的量为$\frac{27g}{18g/mol}$=1.5mol,根据H元素守恒可知,A中没有H元素,含有氧元素为0.6mol×4+1.2mol-1.5mol=2.1mol.
A.Na3PO4中N(Na):N(P)=3:1,故A错误;
B.Na3PO3中N(Na):N(P)=3:1,故B错误;
C.Na4P2O7 中N(Na):N(P)=2:1,Na5P3O10中N(Na):N(P)=5:3<2:1,所以混合体系中N(Na):N(P)<2:1,所以不可能,故C错误;
D.Na3PO4中N(Na):N(P)=3:1>2:1,Na4P2O7 中N(Na):N(P)=2:1,Na5P3O10中N(Na):N(P)=5:3<2:1,所以混合体系中N(Na):N(P)可能为2:1,Na、P与O原子比例也符合,故D正确;
故选D.
点评 本题考查化学方程式有关计算,涉及质量守恒定律的应用,注意利用平均原子数目之比计算,题目有一定的难度.


科目:高中化学 来源: 题型:解答题
| 试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ① | 取少量该焰火原料加入冷水 | 无明显现象 | 不含Li、Na等活泼金属 |
| ② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体产生,溶液呈无色 | 可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种 |
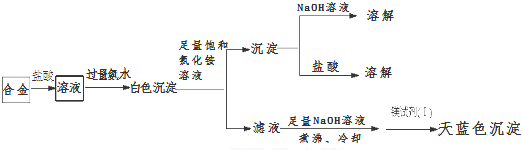

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4L乙烯中C-H键数为4NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+50 kJ•mol-1 | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1 300 kJ | |
| C. | 2C2H2+5O2═4CO2+2H2O△H=-2 600 kJ | |
| D. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2 600 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | Na2O,NaOH,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com