
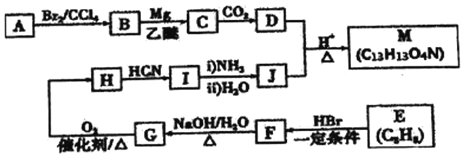
【题目】某有机反应中间体(M)的一种合成路线如下图所示。
已知:①![]()
②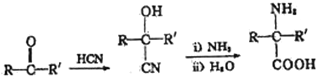 (R表示氢原子或烃基)
(R表示氢原子或烃基)
③标准状况下,气态烃A 的密度是H2的14倍。
④芳香族化合物H能发生银镜反应。
⑤M 中还有一个除苯环之外的环状结构。
(1)B的名称(系统命名)为________;H→I的反应类型为_________。
(2) E 中官能团的结构简式为_________。
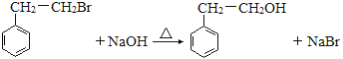
(3)F→G 的化学方程式为_________。
(4)D+J→M的化学方程式为__________。
(5) 写出符合下列条件的J的所有同分异构体的结构简式:_________ (不考虑立体异构)。
①苯环上连有-NO2 ②核磁共振氢谱有3个峰
(6) 结合已有知识和相关信息。写出以CH3CHO和题中的物质为原料制备分子式为C6H10N2O2(含六元环)的物质的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:_____________
![]()
【答案】 1,2—二溴乙烷 加成反应 ![]()
 HOOCCH2CH2COOH+
HOOCCH2CH2COOH+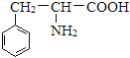
![]()
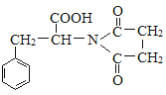 +2H2O
+2H2O 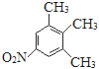 、
、 CH3CHO
CH3CHO![]()
![]()
![]()
【解析】标准状况下,气态烃A的密度是H2的14倍,则Mr(A)=14×2=28,故A为CH2=CH2,A与溴发生加成反应生成B为BrCH2CH2Br,结合信息①可知,C为BrMgCH2CH2MgBr,D为HOOCCH2CH2COOH;E的分子式为C8H8,系列反应得到芳香族化合物H能发生银镜反应,故E为芳香烃,E与HBr发生加成反应得到F,则E为![]() ,F水解得到G,G发生催化氧化得到H,故F为
,F水解得到G,G发生催化氧化得到H,故F为![]() ,G为
,G为![]() ,H为
,H为![]() ,由信息②可知I为
,由信息②可知I为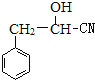 ,J为
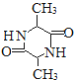
,J为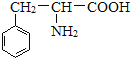 ,M中还有一个除苯环之外的环状结构,结合M的分子式可知,D与J脱去2分子水生成M,故M的结构简式为
,M中还有一个除苯环之外的环状结构,结合M的分子式可知,D与J脱去2分子水生成M,故M的结构简式为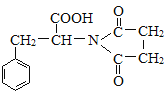 。
。
(1)B为BrCH2CH2Br,系统命名为1,2-二溴乙烷;H→I的反应类型为加成反应,
故答案为:1,2-二溴乙烷;加成反应;
(2)E为![]() ,官能团的结构简式为
,官能团的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)F→G的化学方程式为: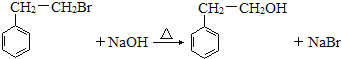 ,
,
故答案为: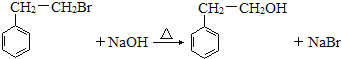 ;
;
(4)D+J→M的化学方程式为:HOOCCH2CH2COOH+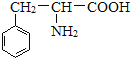
![]()
 +2H2O,故答案为:HOOCCH2CH2COOH+
+2H2O,故答案为:HOOCCH2CH2COOH+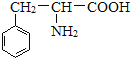
![]()
 +2H2O ;
+2H2O ;
(5) J为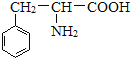 。①苯环上连有-NO2,②核磁共振氢谱有3个峰,对称性较高,符合条件的J的同分异构体有:
。①苯环上连有-NO2,②核磁共振氢谱有3个峰,对称性较高,符合条件的J的同分异构体有: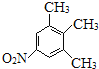 、
、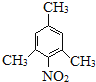 ,故答案为:
,故答案为: 、
、 ;
;
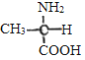
(6)根据题干流程图M的合成可知,分子式为C6H10N2O2(含六元环)的物质的结构中可能含有2个肽键,结构简式可能为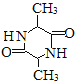 。以CH3CHO和题中的物质为原料合成
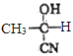
。以CH3CHO和题中的物质为原料合成 ,可以首先根据信息②,让CH3CHO与HCN加成生成
,可以首先根据信息②,让CH3CHO与HCN加成生成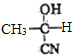 ,再生成
,再生成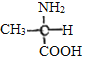 ,最后2分子
,最后2分子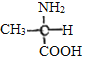 通过成肽反应生成
通过成肽反应生成 即可,合成路线为CH3CHO
即可,合成路线为CH3CHO![]()

![]()
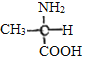
![]()
 ,故答案为:CH3CHO
,故答案为:CH3CHO![]()

![]()
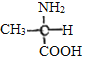
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】在透明溶液中能大量共存的一组离子是( )
A.NH4+、Ba2+、Br-、CO32-B.Cl-、S2-、Fe2+、H+
C.Na+、H+、NO3-、HCO3-D.K+、Na+、SO42-、MnO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。水中溶解氧的测定步骤如下:
(1)向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;
(2)加入适量稀H2SO4,搅拌,等MnO(OH)2与I-完全反应生成Mn2+和I2后;
(3)用Na2S2O3标准溶液滴定至终点。
测定过程中物质的转化关系如下:
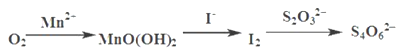
已知:MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O 2S2O32- +I2= S4O62-+2I-
①加入稀硫酸后搅拌的作用是__________;Na2S2O3标准溶液应装在______________滴定管中(填酸式或碱式)。
②滴定过程中以_____________为指示剂;达到滴定终点的标志为____________________。
③写出O2将Mn2+氧化成MnO(OH)2的离子方程式____________________;
④若加入的稀H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生误差的一个原因(用离子方程式表示)__________________。
⑤下列操作使测得水样中溶氧量(DO)比实际值偏高的是__________________。
A.第(1)步操作静置时没有密封 B.装Na2S2O3标准溶液的滴定管没有润洗
C.滴定前锥形瓶洗净后没有干燥 D.滴定前读数正确,滴定后俯视读数
⑥取加过一定量CaO2·8H2O的池塘水样l00.00mL,按上述方法测定水中溶解氧量,消耗0.01000
mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为____________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解下列电解质溶液,有关叙述正确的是( )
A. 等物质的量浓度的NaCl和AlCl3混合液完全电解后,所得的混合液的pH值增大
B. NaCl溶液电解一定时间后,要恢复到电解前状态,应加入适量盐酸
C. Na2SO4溶液在电解过程中,阴极区pH值降低
D. 电解CuSO4溶液,阳极反应式为:2H2O+O2+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是( )
CH3OH(g) 达到平衡。下列说法正确的是( )
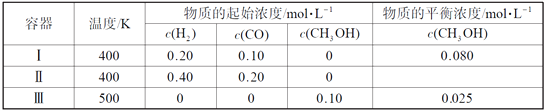
A. 该反应的逆反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外。将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口。充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液。试回答:
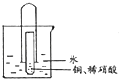
(1)写出铜片溶于稀硝酸的离子方程式________。
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及________。
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后小试管内溶 液中NO ![]() 物质的量浓度为________mol/L(忽略溶液体积变化)。
物质的量浓度为________mol/L(忽略溶液体积变化)。
(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方程式________。
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?________(填“正确”或“不正确”),理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保持洁净安全的生存环境已成为全人类的共识。
(1)家庭装修所用的复合板材中常会放出对人体有严重危害的物质,这种有害物质主要是指________(填名称)。
(2)天然水中含有的细小悬浮颗粒可以用明矾做进行净化处理,明矾水解得到的________可以吸附细小悬浮颗粒。
(3)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.为控制大气中二氧化硫的排放,常采取的措施是在煤炭中加入石灰石粉末对化石燃料进行脱硫处理,其原理用方程式可表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如右下图(二茂铁熔点是173℃,在100℃时开始升华;沸点是249℃)。实验步骤为:
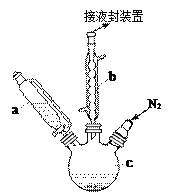

①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是_________,作用是_________________________。
(2)步骤①中通入氮气的目的是________________________________。
(3)仪器c的适宜容积应为______:①100ml、②250ml、③500ml;仪器a使用前应进行的操作是_____,其操作过程为:关闭恒压滴液漏斗颈部旋塞_______________________。
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为________________________________;步骤⑦是二茂铁粗产品的提纯,该过程在右图中进行,其操作名称为__________。
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是_____。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为_______(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下图两种化合物的结构或性质描述正确的是( )
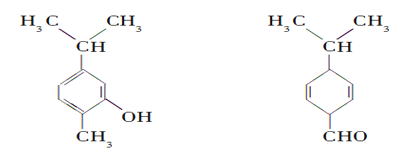
A. 不是同分异构体
B. 分子中共平面的碳原子数相同
C. 均能与溴水反应
D. 可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com