
25 ℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说 法正确的是
法正确的是
A.BOH溶于水,其电离方程式是BOH===B++OH-
B.若一定量的上述两溶液混合后pH=7,则c(A-)=c(B+)
C.在0.1 mol·L-1 BA溶液中,c(B+)>c(A-)>c(OH-)>c(H+)
D.若将0.1 mol·L-1 的BOH溶液稀释至0.001 mol·L-1,则溶液的pH=9
科目:高中化学 来源:2015-2016学年江西省高二上二次月考化学试卷(解析版) 题型:选择题
下列事实中不能用勒夏特列原理加以解释的是( )
A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深
B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体
C.夏天,打开啤酒瓶时会在瓶口逸出气体
D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
0.1mol/L体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lgV/V0的变化如图所示,下列叙述错误的是( )
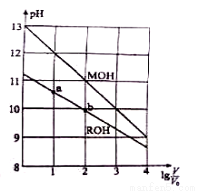
A.ROH的电离方程式为ROH=R++OH-
B.ROH的电离程度:b点大于a点
C.等pH的ROH和MOH溶液,则MOH的浓度低
D.当lgV/V0=2时,若两溶液同时升高温度,则
C(R+)增大,C(M+)不变。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃会宁第一中学高三上第三次月考理化学试卷(解析版) 题型:选择题
进入人体的O2有2%转化为“活性氧”,它能加速人的衰老,被称为“生命杀手”,服用亚硒酸钠(Na2SeO3)能消除人体内的“活性氧”。下列说法正确的是 ( )
A.Na2SeO3在反应中做氧化剂 B.Na2SeO3在反应中做还原剂
C.亚硒酸钠中硒的化合价为+6价 D.“活性氧”在反应中做催化剂
查看答案和解析>>
科目:高中化学 来源:2016届安徽马鞍山、淮北、铜陵四校高三上第三次联考化学试卷(解析版) 题型:实验题
【化学—选修2:化学与技术】
金属钒素有“合金维生素”之称,普通钢中加入少量的钒(V)能极大地改善钢的弹性和强度。工业上回收废钒催化剂(含有V2O5、VOSO4、K2SO4、SiO2)中的钒的主要流程如下:
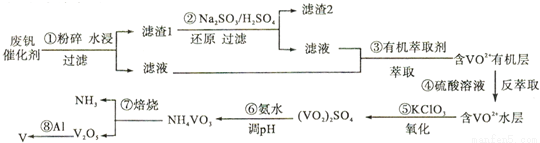
回答下列问题:
(1)滤渣l的主要成分是________________;
(2)步骤②中发生反应的离子方程式为________________;
(3)步骤③的变化过程可简化为(HA表示有机萃取剂)
VOSO4+(水层)+2HA2(有机层) VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
(4)该工艺流程中,可以循环利用的物质除了氨气以外,还有____________;
(5)调节溶液pH,可将(VO2)SO4转变成NH4VO3沉淀;25℃时,当PH为1.7~1.8时,钒沉淀率为98.8%;假设其它各步反应都完全进行,已知KC1O3的还原产物是KCl,若每消耗1moiKC1O3,理论上可回收金属钒___________g(计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:选择题
下列叙述正确的是
A.同温同压下,相同体积的物质,其物质的量一定相等
B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.相同条件下的一氧化氮气体和氮气,若体积相等,则质量一定相等
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:实验题
氮化铝(AlN)是一种新型无机非金属材料,其制取原理为:
Al2O3+3C+N2 2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
为了分析某AlN样品的组成,某实验小组进行了如下探究。
【实验1】测定样品中氮元素的质量分数。
取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).
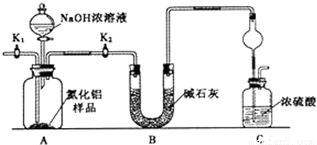
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(1)如图C装置中球形干燥管的作用是__________________________。
(2)完成以下实验步骤:组装好实验装置,首先___________,再加入实验药品.然后______,
打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,缓缓通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__________。
(3)若去掉装置B,则导致测定结果____________(填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_______________________。
【实验2】按以下步骤测定样品中铝元素的质量分数。
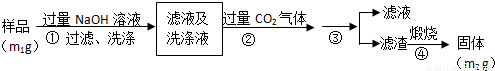
(4)步骤②生成沉淀的离子方程式为___________________。
(5)操作③需要的玻璃仪器有__________________________。
(6)A1元素的质量分数为________(用m1、m2表示)。
【实验3】测定样品中碳元素的质量分数。
称取10.00g样品置于反应器中,通往2.24LO2,在高温下充分反应后得到3.36L气体(AlN不跟O2反应),测得其密度为1.61g•L-1(体积及密度均已换算成标准状况)。
(7)计算该样品中碳元素的质量分数_____________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:选择题
人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图,下列有关说法正确的是( )
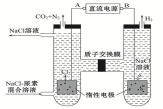
A.B为电源的正极
B.电解结束后,阴极室溶液的pH与电解前相比将升高
C.电子移动的方向是B→右侧惰性电极→质子交换膜→左侧惰性电极→A
D.阳极室中发生的反应依次为2Cl﹣﹣2e﹣=Cl2↑、CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第三次模拟考试理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
铁是最常见的金属材料。铁能形成 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等多种配合物。
(1)基态Fe3+的M层电子排布式为 ;
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式分别是 、 ;
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。 Fe(CO)x常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(4)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为 ,如果铁的原子半径为a cm,阿伏加德常数的值为NA,则此种铁单质的密度表达式为 g/cm3。
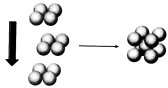
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com