
【题目】114号元素Fl(中文名“![]() ”)是主族元素,其原子核外最外层电子数是4。下列说法错误的是
”)是主族元素,其原子核外最外层电子数是4。下列说法错误的是
A. Fl的原子核外有114个电子B. Fl是第七周期第IVA族元素
C. Fl单质可能是半导体材料D. Fl的原子半径大于同主族其他元素
科目:高中化学 来源: 题型:
【题目】铝是最重要的金属之一,铝及其化合物在生活中有广泛的用途。
(1)纳米铝粉可以作高效催化剂、导电膜层、高档金属颜料等。普通铝在空气中能稳定存在,而纳米铝粉在空气中能自燃,从影响反应速率的角度分析其原因是________。
(2)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①该反应的化学方程式为_________________。
②MnO2加入酸化后的H2O2溶液中,MnO2溶解,同时产生无色无味的气体。该反应的离子方程式是_____________,该反应中还原剂是___________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O将产生的气体通过下图所示装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O将产生的气体通过下图所示装置。
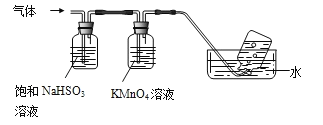
①集气瓶中收集到的气体是_________(填化学式)。
②B中酸性KMnO4溶液褪色(MnO4—还原为Mn2+),发生反应的离子方程式为__________。
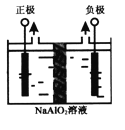
(4)Al(OH)3是重要化工原料。电解法制备高品质Al(OH)3的装置如图(中间用离子交换膜隔开),电解总反应方程式为4NaAlO2+10H2O![]() 4Al(OH)3↓+4NaOH+O2↑+2H2↑,阳极的电极反应式为____________。
4Al(OH)3↓+4NaOH+O2↑+2H2↑,阳极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的说法中,不正确的是
A.与其他分散系的本质区别是能否发生丁达尔效应
B.分散质粒子直径在10-9~l0-7 m之间
C.分散质粒子能穿过滤纸
D.属于介稳体系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是
A.烧碱﹑纯碱﹑碱石灰都是碱B.BaSO4﹑C2H5OH﹑氨水都是电解质
C.硝酸、硫酸、次氯酸都是酸D.CaO﹑Na2O2﹑K2O都是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结构化学从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质。
(1)下列说法正确的是 ______(填字母)。
A、元素电离能由大到小的顺序:O>N>C
B、一个尿素(CO(NH2)2)分子中含1个π键和7个σ键
C、氯化钠和氯化铯晶体具有相同的晶胞
(2)根据等电子体原理,羰基硫(OCS)分子的电子式应为______。光气(COCl2)分子内各原子最外层都满足8电子稳定结构,则光气分子的空间构型为____(用文字描述)。
(3)Cu2+基态的电子排布式为______。将硫酸铜溶液蒸发浓缩后降温结晶,析出蓝色晶体,取25.0g晶体置于坩埚中在一定温度下灼烧,测得剩余固体质量始终保持为23.2g,进一步升高灼烧温度,固体变为白色且质量为16.0g,已知该晶体属于配合物(配合物的内界结构比较稳定),推测其合理的化学式可以表示为______。
(4)通常情况下,溶液中的Fe3+比Fe2+稳定,理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二氯化二硫(S2Cl2)是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193K,沸点为411K,遇水水解产生的气体能使品红褪色。下列有关说法正确的是
A. S2Cl2晶体中存在离子键
B. S2Cl2在熔融状态下能导电
C. S2Cl2分子中各原子均达到8电子稳定结构
D. S2Cl2与水反应后生成的气体难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中所含离子的浓度如下表,则 M 离子可能为 ( )
所含离子 | NO3- | SO42- | H+ | M |
浓度/(molL-1) | 2 | 1 | 2 | 1 |
A.Cl-B.Ba2+C.Na+D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如下图所示(已知A、B、C均为气体)。
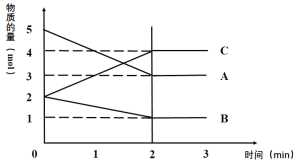
(1)该反应的化学方程式为__________________。
(2)反应开始至2分钟时,B的平均反应速率为______________。
(3)能说明该反应已达到平衡状态的是_________。
A.υ(A)=2υ(B) B.容器内气体密度不变 C.υ逆(A)=υ正(C)
D.各组分的物质的量相等 E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为________。
II.已知甲烷燃烧的化学反应方程式为CH4+2O2![]() CO2+2H2O,若以4mol/L 500mL KOH(aq)为电解质溶液,将其设计为原电池,则
CO2+2H2O,若以4mol/L 500mL KOH(aq)为电解质溶液,将其设计为原电池,则
(1)其正极电极方程式为___________。
(2)至某时刻溶液中c(CO32-)=1mol/L,则导线上通过的电子的物质的量为_____,此时消耗标准状况下CH4体积_____ L 。(假设化学能全部转化为电能;溶液体积保持不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com