
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:

回答下列问题:
(1)葡萄糖的分子式为__________。
(2)A中含有的官能团的名称为__________。
(3)由B到C的反应类型为__________。
(4)C的结构简式为__________。
(5)由D到E的反应方程式为______________。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠反应可释放出2.24 L二氧化碳(标准状况),F的可能结构共有________种(不考虑立体异构),其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为_________。
【答案】 C6H12O6 羟基 取代反应 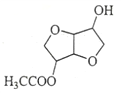
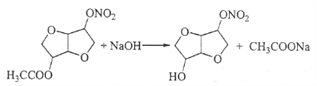 9
9 ![]()
【解析】分析:葡萄糖在催化剂作用下与氢气发生醛基的加成反应生成A,A在浓硫酸的作用下发生分子内脱水反应生成B,B与乙酸发生酯化反应生成C,根据C与D的分子式可知C生成D是C分子中另一个羟基与硝酸发生酯化反应,D在氢氧化钠溶液中水解生成E,据此解答。
详解:(1)葡萄糖的分子式为C6H12O6。
(2)葡萄糖在催化剂作用下与氢气发生醛基的加成反应生成A,因此A中含有的官能团的名称为羟基。
(3)由B到C发生酯化反应,反应类型为取代反应。
(4)根据B的结构简式可知C的结构简式为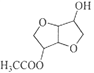 。
。
(5)由D到E是乙酸形成的酯基水解,反应方程式为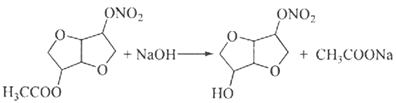 。
。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠可释放出2.24 L二氧化碳(标准状况),说明F分子中含有羧基,7.30 g F的物质的量是7.3g÷146g/mol=0.05mol,二氧化碳是0.1mol,因此F分子中含有2个羧基,则F相当于是丁烷分子中的2个氢原子被羧基取代,如果是正丁烷,根据定一移一可知有6种结构。如果是异丁烷,则有3种结构,所以可能的结构共有9种(不考虑立体异构),即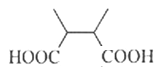 、
、![]() 、
、 、
、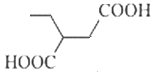 、
、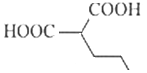 、
、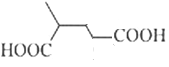 、
、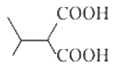 、
、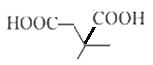 、
、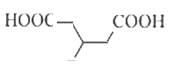 。其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为
。其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为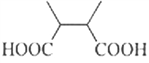 。
。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是 ( )

A. 电池工作时Na+从b极区移向a极区
B. 每消耗3 mol H2O2,转移3 mol e-
C. b极上的电极反应式为:H2O2+2e-+2H+=2H2O
D. a极上的电极反应式为:BH4—+8OH--8e-=BO2—+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。
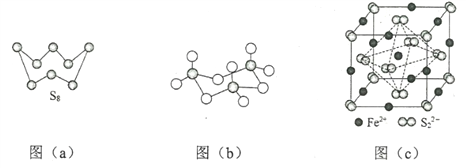
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在K2Cr2O7+14HCl===2KCl+2CrCl3+3Cl2↑+7H2O反应中。
(1) ________元素被氧化,________是氧化剂。
(2)________是氧化产物,________发生氧化反应。
(3)用双线桥法标明电子转移的方向和数目___________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室检验某溶液中是否含有SO42-的操作方法是:_______________________;实验室检验某溶液中是否含有Cl-的操作方法是:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)8羟基喹啉被广泛用作金属离子的络合剂和萃取剂,也是重要的医药中间体。下图是8羟基喹啉的合成路线。

已知:i. 
ii.同一个碳原子上连有2个羟基的分子不稳定。
(1)按官能团分类,A的类别是__________。
(2)A→B的化学方程式是____________________。
(3)C可能的结构简式是__________。
(4)C→D所需的试剂a是__________。
(5)D→E的化学方程式是__________。
(6)F→G的反应类型是__________。
(7)将下列K→L的流程图补充完整:____________

(8)合成8羟基喹啉时,L发生了__________(填“氧化”或“还原”)反应,反应时还生成了水,则L与G物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制氨气常用以下两种方法:
①用固体氢氧化钙与氯化铵晶体反应制取;
②用固体生石灰与浓氨水混合制取。
请回答下列问题:
(1)写出方法①的化学方程式_______________。
(2)方法②能制取氨气的原理是___________________。
(3)检验氨气是否收集满的方法是______________________。
(4)通常用于证明氨气极易溶于水的实验是______________;氨水显碱性的原因是_____________。
(5)制备氨气的装置如下,方法①应选用_________(填字母,下同),方法②应选用__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com