
【题目】用-C4H9的烷烃基取代甲苯苯环上的一个氢原子,能得到的有机物种数为
A. 3种 B. 8种 C. 9种 D. 12种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列除杂质的操作方法中不正确的是
A.NO中有少量的NO2:用水洗涤后再干燥
B.食盐中有少量的NH4Cl:直接加热
C.N2 中有少量的O2:通过灼热的铜网
D.Na2CO3中混有NH4HCO3:加过量的NaOH溶液加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备Cu2(OH)2CO3,其工艺流程如下:
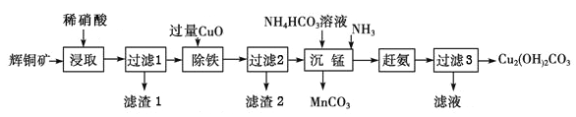
(1)“酸浸”过程中,将矿石粉碎,其目的是__________;加热能加快矿石粉“酸浸”速率,但温度不宜过高,其原因是__________。
(2)Cu2S和硝酸反应,其还原产物为NO。已知1 mol Cu2S完全反应时转移10 mol电子。写出该反应的离子方程式:_____________________。
(3)“除铁”中加入过量氧化铜发生反应的离子方程式为___________________。
(4)从过滤3得到的滤液中可提取一种肥料,它的化学式为__________;滤渣1的主要成分是__________(填化学式)。
(5)设计实验确认过滤2得到的滤液中是否有Fe3+:___________________________。
(6)取wg辉铜矿经上述流程转化,加入agCuO,滤渣2含bgCuO,最终得cmolCu2(OH)2CO3不考虑铜元素损失)。原辉铜矿含Cu2S的质量分数为____________。(用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.92 g Cu和一定量的浓HNO3反应,随Cu不断减少,反应生成气体的颜色逐渐变浅,当Cu 完全消耗时,共收集到气体1.12 L(标况),反应中消耗HNO3物质的量为( )
A. 无法计算 B. 0.11 mol C. 0 .65 mol D. 0.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定的密闭容器中,充入一定体积的CO2和H2,发生反应:CO2(g)+3H2(g)![]() CH3OH (g)+H2O(g)。测得不同温度下CO2的物质的量随时间变化如右图。下列说法正确的是( )
CH3OH (g)+H2O(g)。测得不同温度下CO2的物质的量随时间变化如右图。下列说法正确的是( )

A. 该反应为吸热反应
B. T1、T2对应的平衡常数K1>K2
C. T1时,图中A点的正反应速率小于逆反应速率
D. T2时,若上述反应在压强恒定的密闭容器中进行,达平衡的时间变短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y组成的化合物X2Y,那么X、Y所在主族序数可能是( )
A. ⅡA和ⅦA B. ⅤA和ⅥA C. ⅥA和ⅥA D. ⅠA和ⅥA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种新型、高效的水处理剂,与水反应的化学方程式为:4Na2FeO4+10H2O=4Fe(OH)3+3O2↑+8NaOH。电解制备 Na2FeO4 装置示意图如下。

(1)a是电源的______________极(填“正”或“负”)。电解时,石墨电极附近溶液的碱性____________(填“增强”、“减弱”或“不变”)。
(2)铁电极的反应式为__________________________。
(3)维持一定的电流强度和电解温度,NaOH起始浓度对Na2FeO4浓度影响如下图(电解液体积相同情况下进行实验)。

①电解3.0h内,随NaOH起始浓度增大,Na2FeO4浓度变化趋势是______________(填“增大”、“不变”或“减小”)。
②当NaOH起始浓度为16mol·L-1,1.0~2.0h内生成Na2FeO4的速率是_____________mol·L-1·h-1。
③A 点与B 点相比,n[Fe(OH)3]: A_____________B (填“>”、 “=”或“<” )
(4)提纯电解所得Na2FeO4,采用重结晶、过滤、洗涤、低温烘干的方法,则洗涤剂最好选用______________溶液(填标号)和异丙醇。
A.Fe(NO3)3 B.NH4Cl C.CH3COONa
(5)次氯酸钠氧化法也可以制得Na2FeO4。
己知 2H2(g)+O2(g)=2H2O (1) △H=akJ·mol-1
NaCl(aq)+ H2O(1)=NaClO(aq)+H2(g) △H=bkJ·mol-1
4Na2FeO4(aq)+10H2O(1)=4Fe(OH)3(s)+3O2(g)+8NaOH(aq) △H=c kJ·mol-1
反应 2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(1)的△H=______________ kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法错误的是( )
A. 等质量的H2O与CH2D2含有的质子数相同
B. 室温下CH3COONH4溶液pH=7,1 L 0.1 mol·L-1该溶液中NH![]() 离子数为0.1NA
离子数为0.1NA
C. 标准状况下,6.72 L NO2与水充分反应转移的电子数为0.2NA
D. 1 mol CH3COOC2H5在足量NaOH溶液中水解得到乙醇分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3),又名大苏打,易溶于水,易被氧化,遇酸易分解;其工业制备原理为2Na2S+Na2CO3+4SO2 ==3Na2S2O3+CO2,用途广泛,其中之一为处理含氰化钠的废水。实验室通过如下图所示装置制备Na2S2O3。

(1)实验中生成SO2的化学方程式_________________________________。
(2)b装置的作用是___________________。
(3)反应开始后,c中观察到逐渐析出了淡黄色固体,后又消失的现象,请用离子方程式解释淡黄色固体出现的原因______________________________________。
(4)实验结束后,在e处最好连接盛_________的仪器,目的是___________________。
(5)为了提高产品的产量,通入的SO2不能过量,原因是___________________。
(6)测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
己知:①废水中氰化钠的最高排放标准为0.50 mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I- =AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:取20.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准六AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定终点的现象:_____________________;处理后的废水是否达到排放标准:____________(填“是”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com