
����Ŀ���û�ͭ����Ҫ�ɷ�ΪCu2S��������Fe2O3��SiO2�����ʣ��Ʊ�Cu2(OH)2CO3���乤���������£�
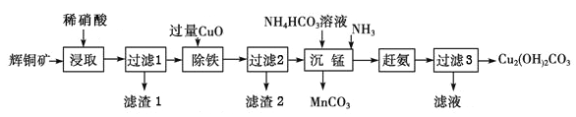
��1��������������У�����ʯ���飬��Ŀ����__________�������ܼӿ��ʯ�ۡ���������ʣ����¶Ȳ��˹��ߣ���ԭ����__________��
��2��Cu2S�����ᷴӦ���仹ԭ����ΪNO����֪1 mol Cu2S��ȫ��Ӧʱת��10 mol���ӡ�д���÷�Ӧ�����ӷ���ʽ��_____________________��
��3�����������м����������ͭ������Ӧ�����ӷ���ʽΪ___________________��
��4���ӹ���3�õ�����Һ�п���ȡһ�ַ��ϣ����Ļ�ѧʽΪ__________������1����Ҫ�ɷ���__________���ѧʽ����
��5�����ʵ��ȷ�Ϲ���2�õ�����Һ���Ƿ���Fe3+��___________________________��
��6��ȡwg��ͭ����������ת��������agCuO������2��bgCuO�����յ�cmolCu2(OH)2CO3������ͭԪ����ʧ����ԭ��ͭ��Cu2S����������Ϊ____________�����ô���ʽ��ʾ��
���𰸡� ���������� HNO3�����ӷ����ֽ� 3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO��+8H2O 2Fe3++3CuO+H2O=2Fe(OH)3+3Cu2+ NH4NO3��(NH4)2SO4 SiO2 ȡ��������Һ���Թ��У��μ�KSCN��Һ�������ɫ������Һ�к���Fe3+��������Fe3+ ![]() ��100%
��100%
�����������������(1)��Ӧ�����ԽС���Ӵ����Խ��ӦԽ�죻�¶�Խ������ӷ����ֽ��ٶ�Խ������2��1 mol Cu2S��ȫ��Ӧʱת��10 mol����������Cu2S������ΪCu2+��SO42-����3������ͭ���������ӣ��ٽ�������ˮ������4����ͭ���̼����˰�������Σ����Դӹ���3�õ�����Һ�к��������SiO2�������Ӧ����5��Fe3+��KSCN��Ӧ��Һ��Ѫ��ɫ����6������ͭԪ�������غ���㡣
��������1����Ӧ�����ԽС���Ӵ����Խ��ӦԽ����������������У�����ʯ���飬��Ŀ�������������ʣ��¶�Խ������ӷ����ֽ��ٶ�Խ�죬�����¶Ȳ��˹��ߡ�
��2��Cu2S����������ΪCu2+��SO42-����Ӧ�����ӷ���ʽ��3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO��+8H2O ��
��3�����������м����������ͭ������ͭ���������ӣ��ٽ�������ˮ������Ӧ�����ӷ���ʽΪ2Fe3++3CuO+H2O=2Fe(OH)3+3Cu2+��
��4������ͭ���̼����˰�������Σ����Դӹ���3�õ�����Һ�к�����Σ��ӹ���3�õ�����Һ�к���NH4NO3��(NH4)2SO4��SiO2�������Ӧ������1����Ҫ�ɷ���SiO2��
��5��ȡ��������Һ���Թ��У��μ�KSCN��Һ�������ɫ������Һ�к���Fe3+��������Fe3+��
��6������ͭԪ�������غ㣬�ܽ�����ͭ�����ʵ���Ϊ![]() mol�� ��Cu2S������Ϊx g
mol�� ��Cu2S������Ϊx g
Cu2S �� Cu2(OH)2CO3
160g 1mol
X g cmol- ![]()
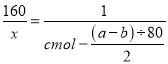
X=160c-a+b������ԭ��ͭ��Cu2S����������Ϊ![]() ��100%��
��100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ1 L���ܱ�������(�������)����1 mol CO2��3 mol H2��һ�������·�����Ӧ��CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ����( )
CH3OH(g)��H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ����( )

A. 3 minǰv����v����3 min��v����v��
B. ���е�3 minʱ������Ӧ���ʺ��淴Ӧ�������
C. 10 min�������и�����Ũ�Ȳ��ٸı�
D. �ﵽƽ����������¶�������Ӧ�����������淴Ӧ���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�У�����֤��A12O3��һ���������Ӽ����ǣ� ��
A. ˮ��Һ�ܵ��� B. �нϸߵ��۵� C. �ۻ�ʱ�ܵ��� D. ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ϢϢ��أ����������������
A.����ʢʳ��B.������������θ����кͼ�
C.��������п������ǿ�俹��ʴ��D.���ؽ������ӵĵ�Ʒ�Һ���������ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ���;�������
A. ��������̫���ܵ�صij��ò��� B. ������ȡˮ���ԭ��
C. ˮ����������ľ�ķ���� D. ����������������ά�IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������SO2 ��Cl2��ֻ�Ϻ�ͨ�����Ʒ����Ȼ�����Һ���۲쵽��������( )
A. ��ɫ�����ɳ��� B. ��Һ������ɫ C. ���ɰ�ɫ���� D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��д�����л���������ƻ�ṹ��ʽ��
�� _______________________________��
_______________________________��
��CH2=C(CH3)CH=CH2_______________________________��
��CH2=CHCOOH _______________________________��
��2,5-����-2,4-����ϩ�Ľṹ��ʽ��_________________________________��
��2��������ֳƻƼ���ҹ��ض�����ҩ������������е�һ���������ҹ���ѧ���о�������ṹ��ͼ��

��������к��������ŵ�������_________________������____________�ࣨ������ӡ�����
�����и����ʣ�
A. 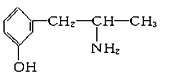 B.
B. 
C.  D.
D. 
E. 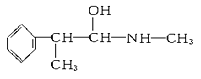
������ػ�Ϊͬ���칹�����________(����ĸ����ͬ)����Ϊͬϵ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����-C4H9��������ȡ���ױ������ϵ�һ����ԭ�ӣ��ܵõ����л�������Ϊ
A. 3�� B. 8�� C. 9�� D. 12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������CH3COOH��NH3��H2O�ĵ��볣����ȣ�����10mLŨ��Ϊ0.01 molL-1�İ�ˮ��Һ�еμ���ͬŨ�ȵ�CH3COOH��Һ���ڵμӹ�������Һ��pH�����Ӵ���������ϵ��ͼ��ʾ�� ��֪100.4=2.5������˵���������

A. n=7
B. ˮ�ĵ���̶��������ټ�С
C. �����´���ĵ��볣��Լ��1.67��10-5
D. Y����Һ��c(NH3��H2O)+c(OH-)=c(CH3COO-)+c(H+)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com