
【题目】用如图所示装置进行铜与浓硫酸反应的实验。

请回答:
(1)铜与浓硫酸反应的化学方程式是______________________。
(2)实验中,观察到品红溶液_____________,石蕊溶液________________________。说明SO2_____________________。(填选项)
a.有氧化性b.有还原性c.有漂白性d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫,还应补充的操作是_________________。
(4)试管D中氢氧化钠溶液的作用是__________,用离子方程式说明___________。
【答案】Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 褪色 变红 cd 加热褪色后的品红溶液 吸收逸出的SO2 SO2+2OH-=SO32-+H2O
CuSO4+SO2↑+2H2O 褪色 变红 cd 加热褪色后的品红溶液 吸收逸出的SO2 SO2+2OH-=SO32-+H2O
【解析】
(1)根据反应物和生成物书写反应的化学方程式;
(2)根据二氧化硫的性质分析判断;
(3)根据二氧化硫的漂白特点分析判断;
(4)根据二氧化硫有毒,需要尾气处理分析。
(1)铜与浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式是Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(2)二氧化硫具有漂白性,能使品红溶液褪色,二氧化硫为酸性氧化物,溶于水显酸性,则石蕊溶液变红,答案选cd;
(3)二氧化硫的漂白是不稳定的、是暂时的,在加热的条件下可以恢复到原来的颜色,所以要检验二氧化硫气体需要加热,若品红溶液恢复红色,则证明是二氧化硫;
(4)二氧化硫有毒,需要尾气处理,又因为二氧化硫能与氢氧化钠溶液反应,则试管D中氢氧化钠溶液的作用是吸收逸出的SO2,反应的离子方程式为SO2+2OH-=SO32-+H2O。


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】下列实验最终能看到白色沉淀的是( )
A.二氧化碳或二氧化硫通入氯化钙溶液中
B.过量二氧化碳通入澄清石灰水中
C.过量二氧化硫通入氢氧化钡溶液中
D.过量二氧化碳通入硅酸钠溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法正确的是
的说法正确的是
A. 该烃属于苯的同系物
B. 所有原子可能都在同一平面上
C. 最多可能有9个碳原子在同一平面
D. 可能有5个碳原子在同一直线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气或氯的化合物的叙述不正确的是( )
A.过量的铁粉与氯气反应生成FeCl3B.少量SO2通入Ca(ClO)2溶液生成CaSO3沉淀
C.氯气能使润湿的淀粉碘化钾试纸变蓝D.次氯酸钙比次氯酸稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是
A. 它是副族元素 B. 它是第六周期元素
C. 它的原子核内有63个质子 D. 它的一种同位素的核内有89个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)石墨晶体中C-C键的键角为_______。其中平均每个六边形所含的C原子数为______个。
(2)金刚石晶体中共价键形成C原子环,每个C被_______个环共用,每条C-C被______个环共用。
(3)CsCl晶体中每个Cs+周围有_______个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有________个。
(4)白磷分子中的键角为__________,分子的空间结构为__________,每个P原子与___个P原子结合成共价键。
(5) 晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____个硼原子组成,共含有_____个B-B键。
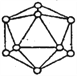
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质(试样中括号内的物质是杂质)时,选用的试剂正确的是( )
A | B | C | D | |
试样 | Na2CO3(NaHCO3) | FeCl2(FeCl3) | Fe(Al) | CO2(SO2) |
除杂试剂 | 澄清石灰水 | NaOH溶液 | NaOH溶液 | 饱和NaHSO3溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的物质,它们之间有如下所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若含金属W的合金是目前用量最大的合金。A是有色气体。
① 指出W在周期表中的位置___________________。
② 向装有C溶液的试管中加入NaOH溶液,观察到的实验现象为________________。过程中发生的氧化还原反应的方程式为__________________。
(2)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46gmol-1。
① B的化学式为______。
② 实验室制取B时,收集方法为__________________________。
③ C与水反应时,氧化剂与还原剂物质的量之比为____________。
(3)若A为淡黄色固体单质,W为气体单质。
① 下列说法正确的是____________
A.A和W的原子价电子数相等
B.A和W对应的元素在自然界既可以以游离态存在,也可以以化合态存在
C.A在过量的W气体中燃烧,可以直接生成C
D.简单氢化物沸点H2A比H2W高
② C溶于水形成化合物D,在加热的条件下,D的浓溶液与A反应的化学方程式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com