
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,可知n(CO2)=$\frac{13.2g}{44g/mol}$=0.3mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,由此可确定有机物分子式,该烃能使酸性高锰酸钾溶液褪色,说明含有碳碳双键,结合结构中只含有一个亚甲基确定烃的结构.
解答 解:完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,可知n(CO2)=$\frac{13.2g}{44g/mol}$=0.3mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,
可知有机物中N(C)=$\frac{0.3}{0.05}$=6,N(H)=$\frac{0.3}{0.05}$×2=12,则有机物分子式为C6H12,该烃能使酸性高锰酸钾溶液褪色,说明含有碳碳双键,若其结构中只含有一个亚甲基,可能为CH2=或-CH2-,则可能的结构有CH2=C(CH3)CH(CH3)2、CH2=CHC(CH3)3、CH3C=C(CH3)CH2CH3、CH3C(CH3)=CHCH2CH3,共4种,
故选B.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,注意把握有机物的结构特点,把握同分异构体的判断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Fe3+、Br-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
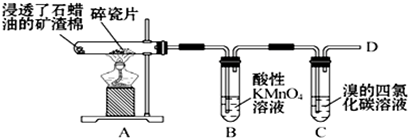
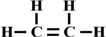 ,空间结构是平面型分子;
,空间结构是平面型分子;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
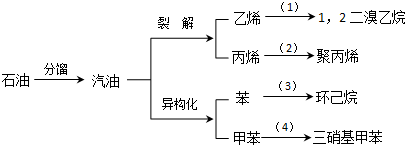
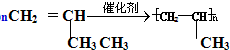 (加成聚合反应)
(加成聚合反应)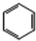 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$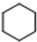 (加成反应)
(加成反应)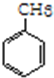 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$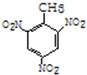 +3H2O(取代反应)
+3H2O(取代反应)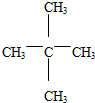 .
. .
.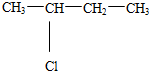 (不考虑顺反异构).
(不考虑顺反异构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛装在敞口玻璃容器中的碘化钾溶液,在空气中久置后,可能会显黄色 | |
| B. | 次氯酸不稳定,见光即分解,可与强碱发生中和反应,则证明次氯酸为弱酸 | |
| C. | 铜粉在氯气中燃烧生成棕色的烟 | |
| D. | 氯水久置后溶液的酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CHO | B. | CH3CH2COOH | C. | CH3COCH3 | D. | CH3CH2OCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.
某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等. | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com