
| A. | 盛装在敞口玻璃容器中的碘化钾溶液,在空气中久置后,可能会显黄色 | |
| B. | 次氯酸不稳定,见光即分解,可与强碱发生中和反应,则证明次氯酸为弱酸 | |
| C. | 铜粉在氯气中燃烧生成棕色的烟 | |
| D. | 氯水久置后溶液的酸性增强 |
分析 A.碘化钾溶液久置显黄色,原因是碘化钾被氧化生成单质碘;
B.次氯酸与强碱溶液发生中和反应,能够证明次氯酸呈酸性,但是不能证明其酸性强弱;
C.铜与氯气燃烧生成氯化铜,同时产生棕黄色烟;
D.次氯酸见光易分解生成氯化氢和氧气,导致酸性增强.
解答 解:A.碘离子具有还原性,易被空气中氧气氧化成碘单质,所以盛装在敞口玻璃容器中的碘化钾溶液,在空气中久置后,可能会显黄色,故A正确;
B.次氯酸不稳定,见光即分解,次氯酸还与强碱发生中和反应,证明次氯酸呈酸性,但是无法证明次氯酸为弱酸,故B错误;
C.铜粉在氯气中燃烧生成氯化铜,有大量棕黄色的烟产生,故C正确;
D.氯水中,氯气与水发生反应Cl2+H2O?HClO+HCl,溶液中含有Cl2、HClO、H2O等分子,次氯酸久置会分解生成HCl,导致酸性增强,故D正确;
故选B.
点评 本题考查了氯溴碘及其化合物性质的综合应用,题目难度中等,明确常见元素及其化合物性质为解答关键,B为易错点,注意掌握判断弱电解质的方法,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 为检验卤代烃中的卤原子,先加入NaOH溶液加热,再加入AgNO3溶液观察颜色变化 | |
| B. | 为制取乙酸乙酯,将稀H2SO4和乙醇、乙酸混合加热,放出的蒸气通入盛有NaOH溶液的试管中 | |
| C. | 为检验醛基的存在,先向试管中加入2mL2%的NaOH溶液和数滴CuSO4溶液,再加乙醛,煮沸 | |
| D. | 为制取乙烯,将稀H2SO4和乙醇混合加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、Na+、NH4+、Fe2+、Ba2+、Cu2+ |
| 阴离子 | OH-、I-、NO3-、AlO2-、HCO3-、HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l) | |
| B. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═BaSO4(s)+H2O(l) | |
| C. | HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l) | |
| D. | HCl(aq)+NH3•H2O(aq)═NH4Cl(aq)+H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 方案 | 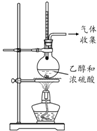 |  | 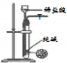 | 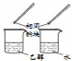 |
| 目的 | 利用乙醇的消去反应制取乙烯 | 蒸发NH4Cl饱和溶液制备NH4Cl晶体 | 制取少量纯净的CO2气体 | 比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| B. | 用稀HNO3清洗试管内壁上的银:Ag+2H++NO3-═Ag++NO2↑+H2O | |
| C. | 实验室盛装NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| D. | 焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com