
| A.2mol H2完全燃烧生成水时放出571.6 kJ的热量 |
| B.1mol 液态水完全分解生成H2和O2时放出285.8kJ的热量 |
| C.2个氢分子和1个氧分子完全燃烧生成液态水时放出571.6 kJ的热量 |
D.上述热化学方程式可表示为H2(g)+ 1/2O2(g)=H 2O (1),△H=-285.8 kJ·mol-1 2O (1),△H=-285.8 kJ·mol-1 |
 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.方程式中化学计量数表示分子数 | B.△H2>0 |
| C.△H2=-△H1 | D.利用△H1、△H2可求出水的气化热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 量。
量。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Na+(g)+Cl-(g)―→NaCl(s);△Q |
| B.Na(s)+Cl2(g)―→NaCl(s);△Q1 |
| C.Na(s)―→Na(g);△Q2 |
| D.Na(g)-e-―→Na+(g);△Q3 |
 ??cC(g)+dD(g),取a mol A和b mol B置于V L密闭容器中,2 min后,测得容器中A的浓度为x mol·L-1,以物质C的浓度变化来表示这段时间内反应的平均速率应为__________ __。
??cC(g)+dD(g),取a mol A和b mol B置于V L密闭容器中,2 min后,测得容器中A的浓度为x mol·L-1,以物质C的浓度变化来表示这段时间内反应的平均速率应为__________ __。查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 催化剂 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2H4+O2=N2+2H2O△H = —534.4kJ/mol |
| B.N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H = —16.7kJ/mol |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H = —534.4kJ/mol |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H = —534.4kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
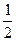 O2(g)=H2O(1) △H=-285.8kJ·mol-1
O2(g)=H2O(1) △H=-285.8kJ·mol-1| A.1:1 | B.1:3 | C.1:4 | D.2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com