
【题目】25℃时,调节2.0×10-3 mol/L氢氟酸水溶液的pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。请结合图中信息回答下列问题:
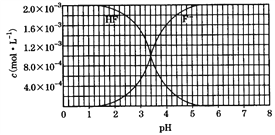
(1)HF电离平衡常数的表达式:Ka=_________。室温下,向HF溶液中滴加NaOH溶液至pH=3.4时,c(F-)∶c(HF) =_______。HF 的电离常数值为_______。
(2)将4.0×10-3mol/L的HF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生:
______________________________。[已知Ksp(CaF2)=1.5×10-10 ]
【答案】 ![]() 1∶1 10-3.4或4.0×10-4(取pH=4时,查图中数据计算得到) c(Ca2+)×c2(F-)=(2.0×10-4)×(1.6×10-3)2=5.12×10-10>Ksp(CaF2),有沉淀产生(F-的浓度根据pH=4查图可得)
1∶1 10-3.4或4.0×10-4(取pH=4时,查图中数据计算得到) c(Ca2+)×c2(F-)=(2.0×10-4)×(1.6×10-3)2=5.12×10-10>Ksp(CaF2),有沉淀产生(F-的浓度根据pH=4查图可得)
【解析】(1)HF电离方程式为HF![]() F-+H+,因此平衡常数的表达式:Ka=
F-+H+,因此平衡常数的表达式:Ka=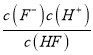 。由图象可知,当pH=4时,c(H+)=1.0×10-4mol/L,c(HF)=4.0×10-3mol/L,c(F-)=1.6×10-3mol/L,则Ka(HF)=
。由图象可知,当pH=4时,c(H+)=1.0×10-4mol/L,c(HF)=4.0×10-3mol/L,c(F-)=1.6×10-3mol/L,则Ka(HF)=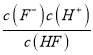 =1×104×1.6×103/4.0×104=4.0×10-4。室温下,向HF溶液中滴加NaOH溶液至pH=3.4时,氢离子浓度是10-3.4mol/L,则根据电离常数可知c(F-)∶c(HF) =
=1×104×1.6×103/4.0×104=4.0×10-4。室温下,向HF溶液中滴加NaOH溶液至pH=3.4时,氢离子浓度是10-3.4mol/L,则根据电离常数可知c(F-)∶c(HF) =![]() 。(2)将4.0×10-3mol/L的HF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节溶液pH=4,此时c(F-)=c(HF)×4.0×104/c(H+)=[2.0×103c(F)]×4.0×104/1×104,解得c(F-)=1.6×10-3(mol/L),c(Ca2+)=2.0×l0-4mol/L,则溶液中c(Ca2+)c2(F-)=2.0×l0-4×(1.6×10-3)2=5.12×10-10>ksp(CaF2)=1.5×10-10,则有沉淀生成。
。(2)将4.0×10-3mol/L的HF溶液与4.0×10-4mol/LCaCl2溶液等体积混合,调节溶液pH=4,此时c(F-)=c(HF)×4.0×104/c(H+)=[2.0×103c(F)]×4.0×104/1×104,解得c(F-)=1.6×10-3(mol/L),c(Ca2+)=2.0×l0-4mol/L,则溶液中c(Ca2+)c2(F-)=2.0×l0-4×(1.6×10-3)2=5.12×10-10>ksp(CaF2)=1.5×10-10,则有沉淀生成。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】该有机物 HOCH2—CH2—CH=CHBr 能发生以下反应中的( )种。
①与 AgNO3 溶液生成淡黄色沉淀 ②加聚反应 ③消去反应 ④使酸性 KMnO4 溶液褪色 ⑤取代反应 ⑥使溴水褪色 ⑦催化氧化反应
A.4B.5C.6D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_____________________。

(2)为防止氯气尾气污染空气,实验室通常用______溶液吸收多余的氯气,原理是__________________。
(用化学方程式表示)。
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是______(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______(填字母,下同)。
A.O2 B.Cl2 C.CO2 D.HClO
(3)一旦发生氯气泄漏和爆炸事故,周围群众应紧急疏散。当人们逃离爆炸现场时,可以用浸有一定浓度某物质水溶液的毛巾捂住鼻子,最适宜采用的该物质是_____________。
A.NaOH B.NaCl C.KCl D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是( )
A. HI和HClOB. HCl和HIO
C. HClO3和HIOD. HClO和HIO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业上常用CO和H2合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) △H
CH3OH(g) △H
①已知:aA(g)+bB(g)=xX(g)+yY(g) △H=x△Hm[X(g)]+y△Hm[Y(g)]-a△Hm[A(g)]-b△Hm[B(g)]。
△Hm[X(g)]表示X(g)的摩尔生成焓,其余类推。25℃101kPa时,CO(g)、H2(g)、CH3OH(g)的摩尔生成焓分别为-110.5kJ·mol-1、0、-201.2kJ·mol-1,则上述反应的△H=_____。
②某温度下,向容积为2L的密闭容器中加入1molCO和2molH2,发生上述反应,CO转化率随时间的变化如图所示:
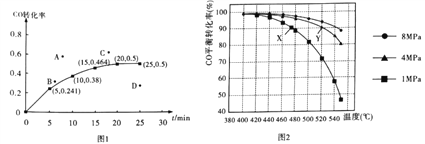
该温度下反应的平衡常数为_______;若起始压强为9MPa,则10min时容器中的压强为_______;若保持其它条件不变,起始时加入2molCO和2molH2,达到平衡,相应的点可能是上图A、B、C、D中的____。
③若只改变反应的一个条件,能使平衡体系中![]() 增大的措施有_______________(答出两点即可)。
增大的措施有_______________(答出两点即可)。
④若投料时CO与H2的物质的量之比恒定,温度、压强对CO平衡转化率的影响如图所示,如图中X点的v(逆)____________Y点的v(正)(填“>”“<”或“=”),理由是_____________。
(2)工业上常用CH3OH来制备HCOOH(甲酸)。已知25℃时,0.1mol·L-1HCOOH溶液的pH为2.3,则甲酸的电离度计算式为______;向0.1mol·L-1HCOOH溶液中加水或加入少量HCOONa晶体时,会引起同样变化的是_______(填编号)。
A.溶液的pH增大 B.HCOOH的电离程度增大
C.溶液的导电能力减弱 D.溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 分子数为NA的CO和C2H4混合气体的体积约为22.4 L
B. 标准状况下,4.48 L水中含有的氢原子数为0.2 NA
C. 电解水制取H2和O2时,每生成1 mol O2就生成2 NA个H2分子
D. 0.1 L 3.0 mol·L-1的KNO3溶液中含有K+的数目为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关工业生产氯气的说法中正确的是( )
A. 工业上常用电解熔融氯化钠来生产氯气
B. 电解饱和氯化钠溶液可得到金属钠、氯气和氢气
C. 每生产1t氯气同时可得1t氢气
D. 电解饱和食盐水制氯气的工业又称“氯碱工业”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液 由于浓度不同而能发生不同氧化还原反应的是
A.①③ B.③④ C.①② D.①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com