

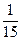
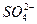 ====BaSO4��
====BaSO4��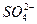 )=n��Ba(OH)2��="0.02" L��0.1 mol��L-1=2��10-3 mol
)=n��Ba(OH)2��="0.02" L��0.1 mol��L-1=2��10-3 mol 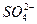 )="0.002" mol
)="0.002" mol ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 N2(g)+O2(g)====NO2(g) ��H��+34 kJ��mol-1���÷�ӦΪ_____________�������ȡ������ȡ�����Ӧ��
N2(g)+O2(g)====NO2(g) ��H��+34 kJ��mol-1���÷�ӦΪ_____________�������ȡ������ȡ�����Ӧ��| ��ѧ�� | ���ܣ� kJ��mol-1�� | ��ѧ�� | ���ܣ� kJ��mol-1�� |
| N��N | 942 | H��O | 460 |
| N��H | 391 | O==O | 499 |
| H��H | 437 | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ͬ��ԭ���γɵķ��ӣ���ԭ�Ӽ�Ļ�ѧ��һ���ǹ��ۼ� |
| B���ǽ���Ԫ�ص�ԭ��֮���γɵĻ�ѧ��һ���ǹ��ۼ� |
| C�������Ǻ����ỹ�������ᣬ������ԭ�Ӽ�Ļ�ѧ�����ǹ��ۼ� |
| D�����Dz�������Ԫ�صĻ�����һ���ǹ��ۻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 H2(g)+
H2(g)+ Cl2(g)="===HCl(g)" ��H2="-x" kJ��mol-1�е�x��ֵ�Ƕ��٣�
Cl2(g)="===HCl(g)" ��H2="-x" kJ��mol-1�е�x��ֵ�Ƕ��٣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������������������Һ��ӦH++OH-====H2O |
B��ϡ����������������Һ��ӦH++ +Ba2++OH-====BaSO4��+H2O +Ba2++OH-====BaSO4��+H2O |
| C������ͭ��Һ������Һ��Ϸ�ӦCu2'++S2-====CuS�� |
D���Ȼ�粒�������ʯ�һ�ϼ��� +OH-====NH3��+H2O +OH-====NH3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SiH4 | B��CH4 | C��H2O | D��NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��BeCl2 | B��H2O | C��CH4 | D��BF3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Fe������ۻ�ϼ��� |
| B�������½����������������Ȼ�立�ĩ��Ϸ�Ӧ |
| C������ƬͶ�뵽ϡ������Һ�� |
| D��Al����NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CO��g����ȼ������283.0KJ/mol,���ʾCO��g��ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ�� CO��g��+1/2 O2��g��= CO2��g������H=��283.0KJ/mol |
| B��ϡ�����ϡ����������Һ��Ӧ���к���Ϊ57.3KJ/mol,���ʾϡ������ϡ�������� ��Һ������Ӧ���Ȼ�ѧ����ʽΪ��H+ (aq) + OH-(aq) = H2O(l)����H=��57.3KJ/mol |
| C�����ȷ�Ӧ�Ƿ��ȷ�Ӧ������Ҫ�㹻����������ʹ��Ӧ���� |
| D��ˮ�ĵ�����������ȹ��̣������¶ȣ�ˮ�����ӻ�����PH��С |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com