
| A. | 相同条件下,2mol H2完全燃烧时液态水放热572kJ | |
| B. | 相同条件下,2mol H2O完全分解吸收热量572kJ | |
| C. | 相同条件下,1mol H2充分燃烧生成气态水放热大于286kJ | |
| D. | 形成1mol H2O的化学键所释放的能量大于断裂lmol H2和0.5mol O2的化学键所吸收的总能量 |
分析 在25℃,101kPa下,1molH2充分燃烧生成液态水放热286kJ,该反应的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-286kJ/mol,
A.氢气的燃烧热为286kJ/mol,据此计算出燃烧2mol氢气放出的热量;
B.生成2mol液态水放出的热量与分解2mol水吸收的热量的数值相等,符号相反;
C.气态水具有的能量大于液态水,则1mol H2充分燃烧生成气态水放热小于286kJ;
D.放热反应中,新键形成放出的热量大于旧键断裂吸收的总能量.
解答 解:在25℃,101kPa下,1molH2充分燃烧生成液态水放热286kJ,则氢气的燃烧热为286kJ/mol,
A.2mol氢气完全燃烧生成液态水放出的热量为:286kJ/mol×2mol=572kJ,故A正确;
B.根据A可知2mol氢气完全燃烧生成液态水放出的热量为572kJ,则相同条件下2mol H2O完全分解吸收热量为572kJ,故B正确;
C.气体水具有的能量较高,则相同条件下1mol H2充分燃烧生成气态水放热小于286kJ,故C错误;
D.氢气与氧气的燃烧反应为放热反应,则形成1mol H2O的化学键所释放的能量大于断裂lmol H2和0.5molO2的化学键所吸收的总能量,故D正确;
故选C.
点评 本题考查了反应热与焓变的应用,题目难度中等,明确反应热与化学键断裂、形成中能量变化的关系为解答关键,C为易错点,注意反应物、生成物具有能量与反应热的关系,试题有利于提高学生的分析能力及灵活应用基础知识的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
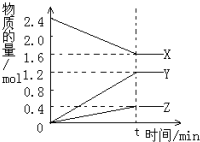 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | p1 | 12.0 | p2 | 24.0 |
| 平衡气体总浓度/10-3mol•L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A. | 混合气体的平均相对分子质量$\overline{M}$不再随时间变化的反应达到平衡状态 | |
| B. | 15.0℃时NH2COONH4(s)分解的平衡常数为2.0×10-9(mol/L)3 | |
| C. | 该反应△H>0,p2=2p1 | |
| D. | 若在恒温下将平衡体系体积减半,再达平衡后,c(NH3)和c(CO2)均比原平衡大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生物质能来源于植物及其加工产品所存贮的能量,绿色植物通过光合作用将化学能转化成生物质能 | |
| B. | 2015年8月国内油价再次迎来成品油最高零售价的下调,上演了年内首场“四连跌”,但油品从国Ⅳ汽油升级到Ⅴ汽油,有助于减少酸雨、雾霾,提高空气质量 | |
| C. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温下可用金属钠还原四氯化钛来制取金属钛 | |
| D. | 元素分析仪可以确定物质中是否含有C、H、O、N、S、Cl、Br等元素,原子吸收光谱可以确定物质中含有哪些金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s)+O2(g)═SO2(g),反应放出的热量大于293.23 kJ•mol-1 | |
| B. | S(g)+O2(g)═SO2(g),反应放出的热量小于293.23 kJ•mol-1 | |
| C. | 1 mol SO2的键能总和大于1 mol硫和1 mol氧气的键能之和 | |
| D. | 1 mol SO2的键能总和小于1 mol硫和1 mol氧气的键能之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol酸与1mol碱完全反应放出的热量就是中和热 | |
| B. | 如果反应在加热时才能发生,则该反应是吸热反应 | |
| C. | 反应物总能量大于生成物总能量,则反应的△H<0 | |
| D. | 强酸强碱中和热的离子方程式可表示为:H+(aq)+OH-(aq)═H2O(l)△H=57.3 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 | |
| B. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| C. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| D. | 防止酸雨发生的重要措施之一是使用清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com