���㣺��ѧ����ʽ���йؼ���,�йػ���ﷴӦ�ļ���
ר�⣺������
�����������ֵ�����ɵĻ�����һ����Ʒ����ϡ����H
2SO
4��ַ�Ӧ��������壬������Ӧ�������������ᷴӦ�ĵ���Ϊ�������������0.56g�������Ϊ1.52g-0.56g=0.96g���������Ħ������ΪM g/mol�����ϼ�Ϊa�����ݵ���ת���غ�
��a=
��2����M=12a��a=2��M=24�������⣬��֪AΪMg��Mg�����ʵ����T
=0.04mol��
�ڶ�����Ʒ����NaOH��Һ��Ӧ��0.896L���弰0.96g������壬������Ϊ���������������Ʒ�Ӧ�ĵ���ΪSi�������ʵ���Ϊ
=0.02mol��
��������Ʒ�ڸ��������¼��ȵõ�һ�������������Mg��Siԭ����Ŀ֮��Ϊ0.04mol��0.02mol=2��1����û�����Ϊ��Mg
2Si��
���������H
3PO
4��Ӧ��0.448L���壬�������ʵ���Ϊ
=0.02mol����ԭ���غ��֪������Ӧ��SiH
4��������������Ӧ��SiH
4+2O
2=SiO
2+2H
2O��0.448LSiH
4��Ӧ��������Ϊ0.896L��ʹ֮��1.000L O
2��ϲ���Ӧ��������Լ1L������90%���������⣬�ݴ˽��
���
�⣺�����ֵ�����ɵĻ�����һ����Ʒ����ϡ����H
2SO
4��ַ�Ӧ��������壬������Ӧ�������������ᷴӦ�ĵ���Ϊ�������������0.56g�������Ϊ1.52g-0.56g=0.96g���������Ħ������ΪM g/mol�����ϼ�Ϊa�����ݵ���ת���غ�
��a=
��2����M=12a��a=2��M=24�������⣬��֪AΪMg��Mg�����ʵ����T
=0.04mol��
�ڶ�����Ʒ����NaOH��Һ��Ӧ��0.896L���弰0.96g������壬������Ϊ���������������Ʒ�Ӧ�ĵ���ΪSi�������ʵ���Ϊ
=0.02mol��
��������Ʒ�ڸ��������¼��ȵõ�һ�������������Mg��Siԭ����Ŀ֮��Ϊ0.04mol��0.02mol=2��1����û�����Ϊ��Mg
2Si����Ӧ����ʽΪ��2Mg+Si
Mg
2Si��
���������H
3PO
4��Ӧ��0.448L���壬�������ʵ���Ϊ
=0.02mol����ԭ���غ��֪������Ӧ��SiH
4��������������Ӧ��SiH
4+2O
2=SiO
2+2H
2O��0.448LSiH
4��Ӧ��������Ϊ0.896L��ʹ֮��1.000L O
2��ϲ���Ӧ��������Լ1L������90%���������⣬
Mg
2Si�������H
3PO
4��Ӧ����SiH
4��Mg��H
2PO
4��
2����ѧ��Ӧ����ʽΪ��Mg
2Si+4H
3PO
4=SiH
4+2Mg��H
2PO
4��
2��
�𣺵����� Mg��Si����������Ʒ���з�Ӧ�ķ���ʽ�У�2Mg+Si
Mg
2Si��Mg
2Si+4H
3PO
4=SiH
4+2Mg��H
2PO
4��
2��SiH
4+2O
2=SiO
2+2H
2O��
���������⿼�������ƶϡ���ѧ����ʽ��д�ȣ��Ѷ��еȣ��ƶ�Ԫ���ǽ���ؼ������ؿ���ѧ����֪ʶ��Ǩ��Ӧ�ã�




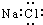
 ������ԭ����ͬһֱ���ϣ�
������ԭ����ͬһֱ���ϣ�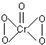 ������������CrΪ+6��
������������CrΪ+6�� ���Ⱥͷ�̪��ˮ�к��л��ܼ��е��ܽ�Ȳ�ͬ�����ܼ�����ֽ������������ʱ�����Ⱥͷ�̪���Բ�ͬ����������ֽ���ƶ����Ӷ��ﵽ�����Ŀ�ģ�ijУ��ѧ��ȤС����ͨ����ԭ�������Ⱥͷ�̪�ӻ����ҺA�з��뿪����
���Ⱥͷ�̪��ˮ�к��л��ܼ��е��ܽ�Ȳ�ͬ�����ܼ�����ֽ������������ʱ�����Ⱥͷ�̪���Բ�ͬ����������ֽ���ƶ����Ӷ��ﵽ�����Ŀ�ģ�ijУ��ѧ��ȤС����ͨ����ԭ�������Ⱥͷ�̪�ӻ����ҺA�з��뿪����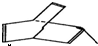 �л���X�Ľṹ�ü���ʽ��ʾ��ͼ
�л���X�Ľṹ�ü���ʽ��ʾ��ͼ
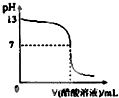 �����£���10mL 0.1mol?L-1NaOH��Һ����μ���0.1mol?L-1������Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������
�����£���10mL 0.1mol?L-1NaOH��Һ����μ���0.1mol?L-1������Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������