
| A、0.2mol?L-1 FeCl3溶液中含有Cl-总数为0.6NA |
| B、次氯酸光照分解产生22.4mL气体(标准状况下),转移电子数为0.002NA |
| C、常温下,4.6g乙醇含有C-H键总数为0.6NA |
| D、常温常压下,4.4g CO2和4.4g N2O的原子总数都是0.3NA |
| ||
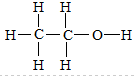 ,乙醇分子中含有5个碳氢键;
,乙醇分子中含有5个碳氢键;
| ||
| 4.6g |
| 46g/mol |
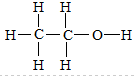 可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;
可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;

科目:高中化学 来源: 题型:
| A、CO2为直线形分子,故CS2也为直线形分子 |
| B、浓硫酸可以干燥HCl气体,故也可用浓硫酸干燥HI气体 |
| C、Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2 |
| D、卤族元素单质随核电荷数增加熔点升高,故碱金属单质熔点也随核电荷数增加而升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2 |
| B、CO2 |
| C、HCl |
| D、NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①②⑤ |
| B、只有①③⑥ |
| C、只有③⑤⑥ |
| D、只有①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.4g CuO粉末 |
| B、5.6g Cu片 |
| C、5.6g Mg条 |
| D、5.6g Zn片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体(FeCl3):NaOH溶液 |
| B、Cl2(HCl):饱和食盐水 |
| C、CO2(SO2):饱和NaHCO3溶液 |
| D、Na2CO3固体(NaHCO3):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com