
【题目】下列实验设计及描述不正确的是
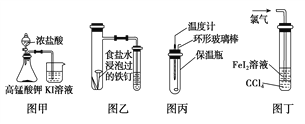
A. 图甲所示的实验,探究氧化性:KMnO4>Cl2>I2
B. 图乙所示的实验,根据小试管中液面的变化判断铁钉发生析氢腐蚀
C. 图丙所示的实验,根据温度计读数的变化用稀盐酸和NaOH溶液反应测定中和热
D. 图丁所示的实验,根据试管中液体颜色的变化比较Cl2、Fe3+、I2的氧化性强弱
科目:高中化学 来源: 题型:
【题目】MnO2用途很广,它是一种广泛应用的氧化剂。例如将它加入熔态的玻璃中,可以除去带色的杂质(硫化物或亚铁盐),称为普通玻璃的“漂白剂”。在锰-锌干电池中用作去极剂,以氧化在电极上产生的氢。
(1)Zn- MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。其电解质溶液呈________性(填“酸”、“碱”或“中”),原因是_________________、________________(用离子方程式表示);该电池工作时,电子流向__________极(填“正”或 “负”)。
(2)工业上,常以菱锰矿(主要成分MnCO3,常含有少量铁、钙、锌等元素)为原料,用电解法可以制备MnO2。其制备过程如下:

写出酸浸的主要化学方程式:______________________。
②下图可以看出,从MnSO4和ZnSO4混合溶液中结晶MnSO4·H2O晶体,需要控制的温度范围为______________(填字母)。
A.0~40℃ B.40~60℃ C.60℃以上

③请写出用惰性电极电解MnSO4溶液制备MnO2的阳极反应:___________________。
④该工艺产生的废水中含有较多的Mn2+,通常用H2S或者Na2S溶液处理。25 ℃,在0.10 mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。

i.pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1;
ii.某溶液含x mol·L-1 Mn2+、0.10 mol·L-1 H2S,当调节溶液pH=5时,Mn2+开始沉淀,则x= 。[已知:Ksp(MnS)=2.8×10-13]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列化学仪器:①托盘天平②玻璃棒③药匙④烧杯⑤量筒⑥500mL容量瓶⑦胶头滴管⑧细口试剂瓶⑨标签纸
(1)现有质量分数为98%、密度为1.84gcm﹣3 的浓硫酸,该浓硫酸的浓度为mol/L.若需要配制500mL 1molL硫酸溶液,需用98%的浓硫酸mL.
(2)定容时加蒸馏水至距刻线处改用加水使溶液的凹液面正好与刻线相平.
(3)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填写“偏高”“偏低”或“无影响”) ①用以稀释硫酸的烧杯未洗涤
②未经冷却趁热将溶液注入容量瓶
③容量瓶中原有少量的蒸馏水
④定容时观察液面俯视 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com