
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯�������Һ����ת����ϵ����֪����B2��C2��D2��E2�ڳ��³�ѹ�¶������壬������G����ɫ��ӦΪ��ɫ��������I��J��Kͨ��״���³���̬������˵����ȷ����
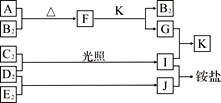
A. B�⻯��ķе������ͬ��������Ԫ���⻯��ķе�
B. ԭ�Ӱ뾶��С��A��C��B��E��D
C. F�мȺ������Ӽ��ֺ��м��Թ��ۼ�
D. G�е�������������ˮ�ĵ���
���𰸡�A
��������I��J��Ӧ������Σ������Ƿֱ���NH3��HX��X����±�أ�����������F��Cl�е�һ�֣���ͬ�����õ��������⻯��ķ�Ӧ����N2��H2��X2����ͬ��Ҫ�ķ�Ӧ��D2ΪH2���ӷ�Ӧ��������H2��X2���Թ�������HX����N2��H2��Ӧ����NH3��Ҫ�ڴ������ȼ�ѹ�����²��ܺϳɣ�����C2ΪX2��E2 ΪN2��IΪHX��JΪNH3��G����ɫ��ӦΪ��ɫ��˵��G���ƵĻ������Ӧ��������K�������G���Ƶ�̼���Σ�������ʽ�Σ���Ӧ����CO2����G���Ƶ��������Σ�������ʽ�Σ���Ӧ����SO2����F���Ƶ���һ�ֻ��������ܹ���CO2����SO2����Ӧ������Ӧ���������࣬ͬ����A��B�к�����Ԫ�أ�����B2�����壬��A�к�����Ԫ�ء������ѧ��Ӧԭ����A��Na���ʣ�B2��O2������������Na2O2��Kֻ����CO2��G��Na2CO3����ΪNa2O2��SO2��Ӧ����Na2SO4����������HCl��Ӧ����SO2���������������A��B���⻯����H2O��Һ̬ʱˮ���Ӽ�����������ͬ���������⻯��֮��ֻ���ڷ��Ӽ�������������ˮ�ķе��ͬ��������Ԫ���⻯��е�ߣ�A��ȷ��B��A��E����Ԫ������ΪNa��O��F��Cl��H��N����CΪF���뾶˳��ΪNa>N>O>F>H����B��������CΪCl���뾶˳��ΪNa> Cl>N>O>H��Ҳ��B������B����C��FΪNa2O2������ʽ��![]() ���Ⱥ������Ӽ��ֺ��зǼ��Թ��ۼ���C����D��GΪNa2CO3��������CO32-��ˮ��Һ���ܹ�����ˮ��Ӷ��ٽ�ˮ�ĵ��룬D������ȷ��A��
���Ⱥ������Ӽ��ֺ��зǼ��Թ��ۼ���C����D��GΪNa2CO3��������CO32-��ˮ��Һ���ܹ�����ˮ��Ӷ��ٽ�ˮ�ĵ��룬D������ȷ��A��


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������еļ��Լ��ں����ߵ������£�����һ���������������˶����Ӷ����������������ЧӦ�����в���������ЧӦ�������
A. CO2B. N2OC. CH4D. N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��A��ͨ�����Cl2 �� �ر�B��ʱ��C���ĺ�ɫ������������������B����C����ɫ��������ɫ����Dƿ��װ���ǣ� �� 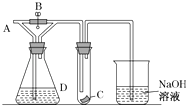
A.ŨH2SO4
B.NaOH��Һ
C.Ũ����
D.����NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǿ������Һ�У����и��������ܴ���������ǣ� ��
A. Fe2+��K+��Cl����NO3�� B. Ag+��Na+��NO3����Cl��
C. Zn2+��Al3+��SO42����Cl�� D. Ba2+��NH4+��Cl����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶ȡ��ݻ���ͬ�������ܱ������з�����ӦN2(g) + 3H2(g)![]() 2NH3(g) ��H= ��92.4kJ/mol������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
2NH3(g) ��H= ��92.4kJ/mol������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
���� | �� | �� | �� |
��Ӧ��Ͷ���� | 1molN2��3molH2 | 2molNH3 | 4molNH3 |
NH3��Ũ��(mol/L) | c1 | c2 | c3 |
��Ӧ�������仯 | �ų�a kJ | ����b kJ | ����c kJ |
��ϵѹǿ | P1 | P2 | P3 |
��Ӧ��ת���� | ��1 | ��2 | ��3 |
����˵����ȷ����
A. 2 c1��c3 B. a + b=92.4 C. 2P1��P3 D. ��1 +��3=1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CO2����ͨ��ˮ�����У�Ȼ��������ɣ����ڸ����³�����գ�������õĹ���������
A. ������
B. ̼���ƣ�������
C. ̼���ƣ���������
D. ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ͼʵ��װ����֤ͨ���ı�Ũ����ʵ�ַ�Ӧ2Fe3++2I-��2Fe2+��I2��Fe3+��Fe2+���ת����K�պ�ʱ��������ָ���һ�η���ƫת����ָ����������ܵμ�0.01mol/L��AgNO3��Һ������ָ��ڶ���ƫת�������෴�������й�˵������ȷ����

A. ָ���һ��ƫתʱ��b����ӦʽΪFe3+��e-��Fe2+
B. ����AgNO3��a����
C. �ڶ���ָ��ƫת��ԭ���ǣ�I-Ũ�ȼ�С����Ӧ�������
D. ��b����0.001 mol Fe3+����ԭʱ����ͨ�����ŵĵ�����Ϊ0.001 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+ CO2(g) ��H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
MgO(s)+SO2(g)+ CO2(g) ��H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
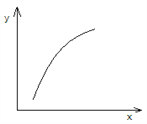
ѡ�� | x | y |
A | �¶� | �����ڻ��������ܶ� |
B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
C | SO2��Ũ�� | ƽ�ⳣ���� |
D | MgSO4������(�������) | CO��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������ϩ���壬����ȥ��ϩ��ѡ�õ��Լ��ǣ� ��
A.����������Һ
B.���Ը��������Һ
C.��ˮ
D.̼������Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com