
| A、汽油和水、CCl4和水两组物质,都能用分液漏斗进行分离 |
| B、在1L 5.0mol/L HCl溶液中取出了10 mL,取出的HCl溶液其浓度为5.0 mol/L |
| C、分散系根据分散质粒子大小可分为溶液、胶体、浊液 |
| D、0.5 molCuO的摩尔质量为40g/mol |


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、实验①中,石墨棒附近的溶液变红色 |
| B、实验②中,上层固体物质是高级脂肪酸 |
| C、实验③中,黑色的氧化铜被乙醇还原成红色的铜 |
| D、实验④中,所用试液只能是含待测元素的盐溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 试 剂 | 保 存 方 法 | 理 由 |
| A | 固体NaOH | 存放在带橡胶塞的广口瓶中 | 防止接触空气被氧化 |
| B | Na2CO3晶体 | 存放在干燥密闭的广口瓶中 | 防止风华呈粉末 |
| C | Na | 保存在乙醇中 | 防止和氧气、水反应 |
| D | AgNO3溶液 | 保存在无色玻璃塞的试剂瓶中,放在阴暗处 | 防止见光分解 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
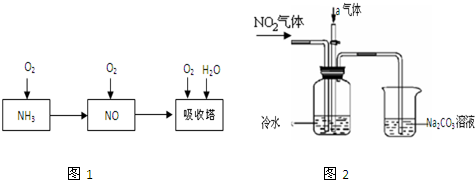
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-、Cl-、Na+ |
| B、SO42-、Cl-、NH4+ |
| C、ClO-、HCO3-、K+ |
| D、I一、Fe2+、Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com