
【题目】(10分)已知水的电离平衡曲线如图示,试回答下列问题:
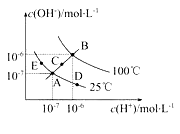
(1)图中五点Kw间的关系是_________________。
(2)若从A点到D点,可采用的措施是________________________。
a.升温 b.加入少量的盐酸 c.加入少量的NH4Cl
(3)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_________________。
(4)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L混合(设混合后溶液的体积等于原两溶液体积之和),所得混合溶液的pH=2,则 V1∶V2=___________________。
(5)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。请回答下列问题(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值______________20.00(填“>”“<”或“=”)。而溶液中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为__________________________。
②如果V=40.00,则此时溶液中c(OH-)-c(H+)-c(CH3COOH)=_______mol·L-1(填数据)
【答案】(1)E=A=D<C<B
(2)bc(3)10:1(各1分)(4)9:11(2分)
(5)①<(1分)c(Na+)=c(CH3COO-)>c(H+)=c(OH-)(2分)②0.033或1/30(2分)
【解析】
试题分析:
(1)Kw只与温度有关,温度升高促进水的电离,Kw增大,因此有E=A=D<C<B;
(2)从A点到D点,溶液由中性转化为酸性,因此选项b和c均符合题意。
(3)25℃时所得混合溶液的pH=7,酸碱恰好中和,即n(OH-)=n(H+),则V(NaOH)×10-5 mol/L=V(H2SO4)×10-4mol/L,得V(NaOH)∶V(H2SO4)=10∶1。
(4)100℃时,Kw=1×10-12,此时pH=11的苛性钠溶液中c(OH-)= ![]() =0.1mol/L,0.05mol/L的稀硫酸中c(H+)=0.1mol/L,混合液的pH=2,则混合液中c(H+)=0.01mol/L,即:
=0.1mol/L,0.05mol/L的稀硫酸中c(H+)=0.1mol/L,混合液的pH=2,则混合液中c(H+)=0.01mol/L,即:![]() =0.01mol/L。解得V1:V2=9:11;
=0.01mol/L。解得V1:V2=9:11;
(5)①若加入20mL氢氧化钠溶液,两溶液恰好完全反应生成CH3COONa,因CH3COO-水解,溶液显示碱性。若要溶液pH=7,则需要氢氧化钠溶液的体积V<20.00mL。因溶液pH=7,即c(H+)=c(OH-),由电荷守恒知:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则c(Na+)=c(CH3COO-),所以c(Na+)=c(CH3COO-)>c(H+)=c(OH-)。
②如果氢氧化钠溶液的体积V=40.00,则根据电荷守恒可得:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),根据物料守恒可得:c(Na+)=2[c(CH3COO-)+c(CH3COOH)],两式相减可得c(OH-)-c(H+)-c(CH3COOH)=[c(CH3COO-)+c(CH3COOH)]= ![]() c(Na+)=0.033mol·L-1
c(Na+)=0.033mol·L-1


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】在容积为 1L的密闭容器中充入1mol CO和2mol H2混合气体,发生以下反应:CO(g)+2H2(g)![]() CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是
CH3OH(g)。T1、T2温度下,CH3OH的物质的量随着时间的变化关系如下图所示。下列有关说法正确的是

A.T1>T2
B.K(T1)>K(T2)
C.T1温度下达到平衡后,再充入一定量CO,CO的转化率增大
D.T2温度下,0~10min间v(H2)=0.06mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已严重已严重危害人类的生活。下列对应关系正确的是
选项 | 环境问题 | 造成环境问题的主要物质 |
A | 酸雨 | O3 |
B | 温室效应 | CO2 |
C | 南极臭氧层空洞 | SO3 |
D | 光化学烟雾 | N2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的叙述正确的是( )
A.所有化学物质内部都存在化学键
B.共价键存在于原子之间,也存在于分子之间
C.离子键是阴、阳离子之间的相互吸引力
D.化学键通常指的是相邻的两个或多个原子间的强烈的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼化钒(VB2)—空气电池是目前储电能力最高的电池,电池示意图如下,该电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5,下列说法正确的是
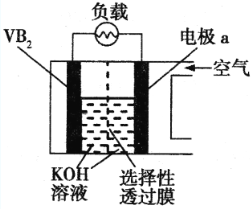
A.电极a为电池负极,发生还原反应
B.每消耗1molVB2转移6mol电子
C.电池工作时,OH向电极a移动
D.VB2极发生的电极反应为:2VB2+22OH-22e=V2O5+2B2O3+11H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4 ![]() 2ClO2↑+ K2SO4+2CO2↑+ 2H2O据此,下列说法不正确的是
2ClO2↑+ K2SO4+2CO2↑+ 2H2O据此,下列说法不正确的是
A.KClO3发生还原反应
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.1molClO2生成,该反应转移的电子数约为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com