
【题目】50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器有___。
(2)烧杯间填满碎纸条的作用是___。
(3)大烧杯上如不盖硬纸板,求得的中和热数值___(填“偏大”“偏小”“无影响”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___;用50mL浓硫酸代替盐酸溶液进行上述实验,测得的中和热的数值会___。(均填“偏大”“偏小”“无影响”)
【答案】环形玻璃搅拌棒 减小实验过程中的热量损失 偏小 偏小 偏大
【解析】
(1)、根据量热计的构造来判断该装置缺少的仪器;
(2)、中和热测定实验成败的关键是保温工作;
(3)、大烧杯上如不盖硬纸板,会使一部分热量散失;
(4)、根据弱电解质电离吸热分析。
(1)、由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
(2)、中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)、大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
(4)、氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,若用50mL浓硫酸代替盐酸溶液进行上述实验,浓硫酸溶于水会放出大量的热,反应放出的热量偏大,测得的中和热的数值会偏大,
故答案为:偏小;偏大。


科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为![]() 的甲、乙两种物质的结构简式如图所示。
的甲、乙两种物质的结构简式如图所示。

(1)甲、乙的化学性质的区别为甲能___________________(填字母,下同),而乙能___________________。
A.被酸性![]() 溶液氧化
溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)![]() 甲和
甲和![]() 乙分别与
乙分别与![]() 发生完全加成反应,甲消耗___________
发生完全加成反应,甲消耗___________![]()
![]() ,而乙消耗__________
,而乙消耗__________![]()
![]()
(3)![]() 还可能有另一种结构丙(如图所示),其二氯代物有___________________种。
还可能有另一种结构丙(如图所示),其二氯代物有___________________种。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可以加同—种物质实现,且E的相对分子质量比D的相对分子质量大16,下列说法正确的是
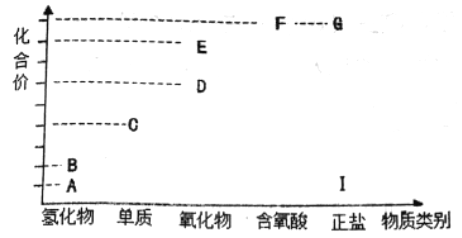
A.汽油燃料中主要含有M元素,所以汽车尾气中通常含有大量D而导致环境问题
B.检验Ⅰ中阳离子的方法:向其样品中加强碱,产生的气体可使湿润的蓝色石蕊试纸变红
C.物质F的浓溶液可以用铁制容器盛放
D.物质B可用作火箭燃料,其电子式为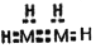
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列叙述正确的是
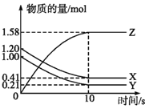
A.反应开始到10 s末时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s末时,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计), 在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g),下列选项不能判断该分解反应已经达到平衡状态的是
A.v 逆(NH3)=2v 正(CO2)
B.密闭容器中氨气的体积分数不变
C.密闭容器中总压强不变
D.密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列事实得出的结论正确的是( )。
选项 | 事实 | 结论 |
A | 甲、乙两种有机物具有相同的相对分子质量和不同的结构 | 甲和乙一定互为同分异构体 |
B | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中, |
C | 在淀粉溶液中加入稀硫酸,水浴加热一段时间后取出部分水解液,滴加银氨溶液后再加热,无银镜出现 | 淀粉的水解产物不具有还原性 |
D | 不存在两种邻二甲苯 | 苯分子中的碳碳键完全相同,苯不是单双键交替结构 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.SO2、SO3都是极性分子
B.在![]() 和[Cu(NH3)4]2+中都存在配位键
和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.金刚石晶体中碳原子以共价键结合,具有键能大、熔点高、硬度大的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、C、N、O元素是与生命活动密不可分的元素,请回答下列问题:
(1)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。已知N2O分子中氧原子只与一个氮原子相连,则N2O的分子空间构型是________。
(2)另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3+O2=2HCl+2COCl2,光气(COCl2)分子的空间构型是________。
(3)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是________(填字母序号)。
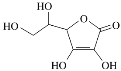
a.分子中既含有极性键又含有非极性键
b.1 mol分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
e.维生素C晶体溶于水的过程中要克服的微粒间作用力只有范德华力
(4)已知尿素的结构简式为H2NCONH2,尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
①基态Fe3+的核外电子排布式为____________。
C、N、O三种元素的第一电离能由大到小的顺序是________。
②尿素分子中C原子和N原子的杂化方式分别是__________。
③[Fe(H2NCONH2)6](NO3)3中H2NCONH2与Fe(+3价)之间的作用力称为__________,与![]() 互为等电子体的一种化合物分子是____________(写化学式)。
互为等电子体的一种化合物分子是____________(写化学式)。
(5)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构简式为
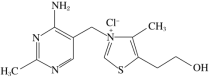
①以下关于维生素B1的说法正确的是________(填字母序号,下同)。
A.只含σ键和π键 B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl D.该物质易溶于盐酸
②维生素B1晶体溶于水的过程中要克服的微粒间作用力有________。
A.离子键、共价键 B.离子键、氢键、共价键
C.氢键、范德华力 D.离子键、氢键、范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CH2Cl2有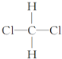 和
和 两种结构
两种结构
B. 分子式为C3H6和C5H10的物质一定互为同系物
C.  的一氯代物有5种
的一氯代物有5种
D. 1mol某烷烃完全燃绕消耗11molO2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com