
ЁОЬтФПЁПНЋвЛЖЈСПДПОЛЕФАБЛљМзЫсяЇЙЬЬхжУгкУмБеецПеШнЦїжа(МйЩшШнЦїЬхЛ§ВЛБфЃЌЙЬЬхЪдбљЬхЛ§КіТдВЛМЦ)ЃЌ дкКуЖЈЮТЖШЯТЪЙЦфДяЕНЗжНтЦНКтЃКNH2COONH4(s)2NH3(g)ЃЋCO2(g)ЃЌЯТСабЁЯюВЛФмХаЖЯИУЗжНтЗДгІвбОДяЕНЦНКтзДЬЌЕФЪЧ
A.v Фц(NH3)ЃН2v е§(CO2)
B.УмБеШнЦїжаАБЦјЕФЬхЛ§ЗжЪ§ВЛБф
C.УмБеШнЦїжазмбЙЧПВЛБф
D.УмБеШнЦїжаЛьКЯЦјЬхЕФУмЖШВЛБф
ЁОД№АИЁПB
ЁОНтЮіЁП
A. ЗДгІNH2COONH4ЃЈsЃЉ![]() 2NH3ЃЈgЃЉ+CO2ЃЈgЃЉЃЌДяЕНЦНКтЪБгІДцдкЃКv Фц(NH3)ЃН2v е§(CO2)Лђепv е§(NH3)ЃН2v Фц(CO2)ЃЌЙЪAе§ШЗЃЛ
2NH3ЃЈgЃЉ+CO2ЃЈgЃЉЃЌДяЕНЦНКтЪБгІДцдкЃКv Фц(NH3)ЃН2v е§(CO2)Лђепv е§(NH3)ЃН2v Фц(CO2)ЃЌЙЪAе§ШЗЃЛ
B. вђЗДгІЮяЪЧЙЬЬхЮяжЪЃЌЫљвдУмБеШнЦїжаNH 3 ЕФЬхЛ§ЗжЪ§ЪМжеВЛБфЃЌЮЊ![]() ЃЌЙЪBДэЮѓЃЛ
ЃЌЙЪBДэЮѓЃЛ
C. ИУЗДгІЪЧЦјЬхЬхЛ§діДѓЕФЗДгІЃЌЙЪЕБШнЦїФкбЙЧПВЛБфЪБЃЌвбДяЕНЦНКтЃЌЙЪCе§ШЗЃЛ
D. гЩгкЗДгІЮяЪЧЙЬЬхЃЌУЛгаДяЕНЦНКтзДЬЌЃЌЦјЬхжЪСПЛсБфЛЏЃЌШнЦїЬхЛ§ВЛБфЃЌУмЖШвВЛсЗЂЩњБфЛЏЃЌЫљвдУмЖШВЛБфЃЌДяЕНСЫЦНКтзДЬЌЃЌЙЪDе§ШЗЃЛ
ЙЪбЁBЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдк10 LУмБеШнЦїжаЃЌ1 mol AКЭ3 mol BдквЛЖЈЬѕМўЯТЗДгІЃК A(g)ЃЋxB(g)![]() 2C(g)ЃЌ2 minКѓЗДгІДяЕНЦНКтЪБЃЌВтЕУЛьКЯЦјЬхЙВ3.4 molЃЌЩњГЩ0.4 mol CЃЌдђЯТСаМЦЫуНсЙће§ШЗЕФЪЧ
2C(g)ЃЌ2 minКѓЗДгІДяЕНЦНКтЪБЃЌВтЕУЛьКЯЦјЬхЙВ3.4 molЃЌЩњГЩ0.4 mol CЃЌдђЯТСаМЦЫуНсЙће§ШЗЕФЪЧ
A. ЦНКтЪБЃЌЮяжЪЕФСПжЎБШn(A)ЁУn(B)ЁУn(C)ЃН2ЁУ11ЁУ4
B. xжЕЕШгк3
C. AЕФзЊЛЏТЪЮЊ20%
D. BЕФЦНОљЗДгІЫйТЪЮЊ0.4 mol/(LЁЄmin)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУГ§ШЅБэУцбѕЛЏФЄЕФЯИТСЬѕНєНєВјШЦдкЮТЖШМЦЩЯЃЈШчЭМЃЉЃЌНЋЩйаэЯѕЫсЙЏШмвКЕЮЕНТСЬѕБэУцЃЌжУгкПеЦјжаЃЌКмПьТСЬѕБэУцВњЩњЁААзУЋЁБЃЌЧвЮТЖШУїЯдЩЯЩ§ЁЃЯТСаЗжЮіДэЮѓЕФЪЧ

A.AlКЭO2ЛЏКЯЗХГіШШСПB.ЯѕЫсЙЏЪЧДпЛЏМС
C.ЩцМАСЫЃК2Al+3Hg2+Ёњ2Al3++3HgD.ЁААзУЋЁБЪЧбѕЛЏТС
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвжазМБИгавдЯТжївЊвЧЦїМАгУЦЗЃЌДѓЪдЙмЁЂДјЕМЙмЕФЕЅПзШћЁЂвЉГзЁЂФїзгЁЂЫЎВлЁЂМЏЦјЦПЁЂВЃСЇЦЌЁЂОЦОЋЕЦЁЂЬњМмЬЈЃЌШчЙћвЉЦЗбЁгУКЯРэЃЌгУвдЩЯвЧЦїгУЦЗЃЌФмЭъГЩЕФЪЕбщгаЃЈ ЃЉ
A.жЦШЁвЛбѕЛЏЕЊB.жЦШЁввЯЉ
C.жЦШЁввШВD.ЧтЦјЛЙдбѕЛЏЭ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙидзгЕФзюЭтФмВуЕФЕчзгХХВМЭМе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A.юыдзгЃК![]()
B.ЬМдзгЃК![]()
C.ТШдзгЃК![]()
D.ТСдзгЃК![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП50mL0.50molЁЄL-1бЮЫсгы50mL0.55molЁЄL-1NaOHШмвКдкШчЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЁЃЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉДгЪЕбщзАжУЩЯПДЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇвЧЦїга___ЁЃ
ЃЈ2ЃЉЩеБМфЬюТњЫщжНЬѕЕФзїгУЪЧ___ЁЃ
ЃЈ3ЃЉДѓЩеБЩЯШчВЛИЧгВжНАхЃЌЧѓЕУЕФжаКЭШШЪ§жЕ___(ЬюЁАЦЋДѓЁБЁАЦЋаЁЁБЁАЮогАЯьЁБ)ЁЃ
ЃЈ4ЃЉгУЯрЭЌХЈЖШКЭЬхЛ§ЕФАБЫЎДњЬцNaOHШмвКНјааЩЯЪіЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс___ЃЛгУ50mLХЈСђЫсДњЬцбЮЫсШмвКНјааЩЯЪіЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс___ЁЃ(ОљЬюЁАЦЋДѓЁБЁАЦЋаЁЁБЁАЮогАЯьЁБ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊдЊЫидзгЕФЯТСаНсЙЙЛђаджЪЃЌФмШЗЖЈЦфдкжмЦкБэжаЮЛжУЕФЪЧ(ЁЁЁЁ)
A. ФГдЊЫидзгЕФЕкЖўЕчзгВуЕчзгХХВМЭМЮЊ![]()
B. ФГдЊЫидкФГжжЛЏКЯЮяжаЕФЛЏКЯМлЮЊЃЋ4
C. ФГдЊЫиЕФдзгзюЭтВуЩЯЕчзгЪ§ЮЊ6
D. ФГдЊЫиЕФЭтЮЇЕчзгХХВМЪНЮЊ5s25p1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМюЪНЬМЫсЭ[Cu(OH)2CuCO3]ЪЧвЛжжгУЭОЙуЗКЕФЛЏЙЄВњЦЗЃЌЪЕбщЪвжЦБИМюЪНЬМЫсЭЕФЗДгІдРэЮЊЃК2CuSO4+2Na2CO3+H2O=Cu(OH)2CuCO3Ё§+CO2Ёќ+2Na2SO4ЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉХфжЦ100mLХЈЖШОљЮЊ0.50molL-1ЕФCuSO4ШмвККЭNa2CO3ШмвКЃЌашвЊгУЕНЕФВЃСЇвЧЦїгаСПЭВЁЂЩеБЁЂНКЭЗЕЮЙмКЭ___ЁЃ
ЃЈ2ЃЉШЁ50mL0.50molL-1CuSO4ШмвКМгШы50mL0.50molL-1Na2CO3ШмвКжаЃЌЗДгІКѓЩеБЕзВПГіЯжДѓСПРЖТЬЩЋГСЕэЁЃЩшМЦЪЕбщжЄУїРЖТЬЩЋГСЕэжаЛьгаФбШмгкЫЎЕФМюЪНСђЫсЭ[Cu2(OH)2SO4]ЃЌЪЕбщВНжшЪЧЃКЙ§ТЫЃЌ___ЁЃ
ЃЈ3ЃЉАДзюМбХфБШ n(CuSO4)ЉUn(Na2CO3)=1ЉU1.2НјааЪЕбщЃЌЗДгІ15minЃЌЫљЕУЪЕбщНсЙћШчЯТЃК
ЮТЖШ/Ёц | 60 | 65 | 75 | 80 | 90 |
ГСЕэСП/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
ЗжЮі75ЁцЪБГСЕэСПзюЖрЕФдвђЃК___ЁЃ
ЃЈ4ЃЉВщдФзЪСЯПЩжЊМюЪНЬМЫсЭЕФзщГЩгаЖржжЃЌПЩгУxCu(OH)2yCuCO3БэЪОЁЃФГаЁзщРћгУвдЯТзАжУВтЖЈФГМюЪНЬМЫсЭбљЦЗЕФзщГЩЃК
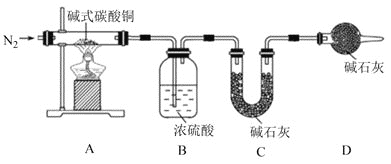
ЂйAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ___ЁЃ
ЂкМгШШЪБГжајЭЈШыN2ЕФФПЕФЪЧ___ЁЃ
ЂлГЦШЁ32.0gбљЦЗЃЌГфЗжЗДгІКѓЕУЕН24.0gВаСєЮяЃЌBдіжи3.6gЃЌCдіжи4.4gЁЃИУбљЦЗЕФЛЏбЇЪНЮЊ___ЁЃШєЖдЕїBКЭCзАжУЕФЮЛжУЃЌ___(ЬюЁАФмЁБЛђЁАВЛФмЁБ)ВтЫуГіИУбљЦЗЕФЛЏбЇЪНЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏКЯЮяМзЁЂввЁЂБћЪЧКЯГЩЯћбзвЉТхЫїТхЗвЕФжаМфЬхЁЃ

ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.МзЗжзгжаЫљгаЬМдзгвЛЖЈДІгкЭЌвЛЦНУц
B.БћЗжзгжаКЌга1ИіЪжадЬМдзг
C.вЛЖЈЬѕМўЯТЃЌМзЁЂввЁЂБћОљФмгыH2ЗЂЩњМгГЩЗДгІ
D.1 molввгызуСПNaOHШмвКГфЗжЗДгІЃЌзюЖрЯћКФNaOHЕФЮяжЪЕФСПЮЊ3 mol
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com