
【题目】化合物甲、乙、丙是合成消炎药洛索洛芬的中间体。

下列说法正确的是
A.甲分子中所有碳原子一定处于同一平面
B.丙分子中含有1个手性碳原子
C.一定条件下,甲、乙、丙均能与H2发生加成反应
D.1 mol乙与足量NaOH溶液充分反应,最多消耗NaOH的物质的量为3 mol
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计), 在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g),下列选项不能判断该分解反应已经达到平衡状态的是
A.v 逆(NH3)=2v 正(CO2)
B.密闭容器中氨气的体积分数不变
C.密闭容器中总压强不变
D.密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是________________;
(2)X与金属钠反应放出氢气,反应的化学方程式是____________(有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是________________;
(4)X与高锰酸钾酸性溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应能生成106 g W,计算该反应的产率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的产物,并进行有关探究实验,回答下列问题:
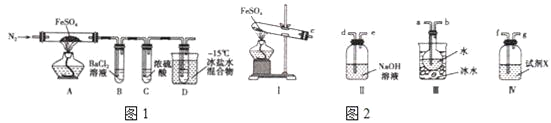
实验一:高温分解FeSO4,利用如图1所示的实验装置进行实验。
已知:①SO2熔点为-72℃,沸点为-10℃;②SO3熔点为-16.8℃,沸点为44.8℃。
(1)连接装置,检验气密性良好,放入药品,通入一段时间N2然后加热,通入N2的目的是___。
(2)隔绝空气加热至650℃,看到B中有白色沉淀,D试管中有无色液体,硬质玻璃管中的固体变为___,同时有两种无色气体生成,写出该反应的化学方程式___。
(3)反应完毕后,停止加热冷却后,取硬质玻璃管中固体,加盐酸,反应的离子方程式是___,将反应后所得溶液滴入D试管中,溶液变为浅绿色,该反应的离子方程式是___。
实验二:探究高温分解FeSO4生成的气体
(4)用如图2所示装置设计实验,验证高温分解FeSO4生成的气态物质
①按气流方向连接各仪器,用字母表示接口的连接顺序:c-___。
②试剂X的名称是___。
③充分反应后,利用装置 III中圆底烧瓶内混合物测定已分解的FeSO4的质量,向圆底烧瓶中逐渐滴入氯化钡溶液,直到沉淀完全;然后过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重.若最终得到沉淀的质量为Wg,则已分解的FeSO4的质量__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜酸镧是一种反铁磁绝缘体,可由Cu(NO3)2和La(NO3)3为起始原料、水为溶剂、柠檬酸为络合剂,采用溶胶—凝胶法制备。
(1)Cu2+基态核外电子排布式为___。
(2)与NO![]() 互为等电子体的阴离子为___。
互为等电子体的阴离子为___。
(3)柠檬酸(结构简式为 )分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。
)分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。
(4)铜酸镧的晶胞结构如图所示,写出其化学式:___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CH2Cl2有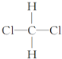 和
和 两种结构
两种结构
B. 分子式为C3H6和C5H10的物质一定互为同系物
C.  的一氯代物有5种
的一氯代物有5种
D. 1mol某烷烃完全燃绕消耗11molO2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍氢电池是二十世纪九十年代发展起来的一种新型绿色电池,具有高能量、长寿命、无污染等特点。用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图1所示。电池的总反应式为:2Ni(OH)2 ![]() H2+2NiO(OH)
H2+2NiO(OH)

(1)①镍氢电池充电时,碳电极连接直流电源的______极。阳极的电极反应式为______
②镍氢电池放电时,OH-移向______(填“碳电极”或“镍电极”)。
(2)除了用纳米碳管等材料储氢外,还可使用有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。一定条件下,利用图2装置可实现有机物的电化学储氢(忽略其它有机物)。
①A为电源的______极。
②电极E上产生的气体为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:__________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______,________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。

(3)仪器A的名称为________,干燥管D的作用是_____________________________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将 2 mol A 和 3 mol B 充入一密闭容器中,发生反应:aA(g)+B(g) ![]() C(g)+D(g),5 min 后达平衡,已知各物质的平衡浓度的关系为 ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的 10 倍,A 的转化率没有发生变化, 则B 的转化率为( )
C(g)+D(g),5 min 后达平衡,已知各物质的平衡浓度的关系为 ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的 10 倍,A 的转化率没有发生变化, 则B 的转化率为( )
A.60%B.40%C.24%D.4%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com