
【题目】次磷酸(H3PO2) 为一元中强酸,具有较强的还原性,可用电渗析法制备,“四室电渗析法”工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。下列叙述不正确的是( )

A. 阳极反应为2H2O-4e-=O2↑+4H+
B. 产品室中发生反应H++ H2PO2-=H3PO2, 该法还可得副产品NaOH
C. 原料室中H2PO2- 向左移动,Na+ 向右移动,该室pH 升高
D. 阳膜1的主要作用是防止H2PO2- 进入阳极室被氧化并允许H+通过
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】离子方程式BaCO3+2H+═CO2↑+H2O+Ba2+中的H+不能代表的物质( ) ①H2SO4②NaHSO4③HNO3④HCl ⑤CH3COOH.
A.①②⑤
B.①④⑤
C.②④⑤
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为下列混合物的分离或提纯提供正确的方法
①除去Ca(OH)2溶液中悬浮的CaCO3微粒
②分离四氯化碳与水的混合物
③分离汽油和煤油
④提纯氯化钠和硝酸钾混合物中的硝酸钾 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.3gNa、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672ml混合气体,将该混合气体通过放电恰好反应,则原混合物中Na、Na2O、Na2O2的物质的量之比为( )
A: 1:2:1 B: 1:1:1 C: 1:3:1 D: 4:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是( )
A.过滤时,玻璃棒的末端应轻轻靠在三层滤纸上
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.称氢氧化钠时,不能直接称量,要放在纸片上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2![]() CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:

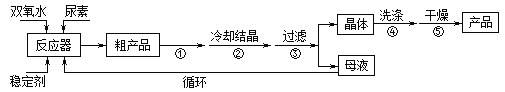
请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在“分子马达”研究方面的成就,一种光驱分子马达结构如图所示。有关该分子的说法正确的是

A. 该分子属于芳香烃
B. 两个苯环可以处于同一平面
C. 能与NaHCO3和酸性KMnO4溶液反应
D. 1mol该分子最多可与2molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
B. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
C. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
D. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g) △H<0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g) △H<0,达平衡后,升高温度体系颜色变深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com