
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的简易流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______________。写出铝氢化钠与水反应的化学方程式_____________________。
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
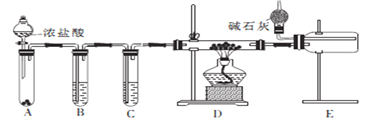
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是________________。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_________________。
(4)丙同学设计以下4种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。
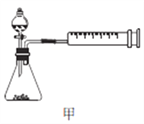
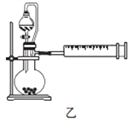
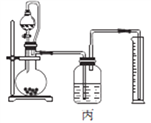
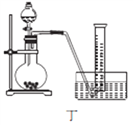
从易操作性、准确性角度考虑,宜选装置________。铝氢化钠与水完全反应,冷却至室温的标志是______。
【答案】 反应放出大量热量使生成的H2迅速膨胀而爆炸 NaAlH4+2H2O═NaAlO2+4H2↑ 吸收剩余的氯气并避免空气中的水蒸气进入D中 先将装置A中的分液漏斗打开,反应一段时间,使D中玻璃管充满黄绿色气体 NaOH溶液(或其他合理答案) Na2O2(或Na等其他合理答案) 乙 连续两次读取的H2体积相等
【解析】(1)NaAlH4与水反应生成NaAlO2和H2,化学方程式为:NaAlH4+2H2O=NaAlO2+4H2↑;由已知①可得,NaAlH4遇水能迅速发生反应,放出大量热使生成的H2迅速膨胀而可能引起爆炸。
(2)由制备无水氯化铝的装置可知,A为“固-液![]() ”制Cl2装置,B为除去Cl2中HCl的装置,C为吸水干燥装置,D为Al和Cl2反应装置,E为收集AlCl3装置。①因为AlCl3遇水能迅速反应,所以E中碱石灰的作用是:吸收剩余氯气和防止空气中的水蒸气进入D中。②点燃装置D处酒精灯之前,先打开装置A中的分液漏斗,反应一段时间,使D中玻璃管充满黄绿色气体,从而排尽装置内的空气。
”制Cl2装置,B为除去Cl2中HCl的装置,C为吸水干燥装置,D为Al和Cl2反应装置,E为收集AlCl3装置。①因为AlCl3遇水能迅速反应,所以E中碱石灰的作用是:吸收剩余氯气和防止空气中的水蒸气进入D中。②点燃装置D处酒精灯之前,先打开装置A中的分液漏斗,反应一段时间,使D中玻璃管充满黄绿色气体,从而排尽装置内的空气。
(3)①若用上述装置制备NaH,只要将A中试剂改为金属锌,B中用NaOH等碱性溶液除去挥发出的HCl气体,D中试剂改为金属钠,就可以达到目的。②该装置无法隔绝氧气,,若操作不当,可能会使NaH中含有Na2O2杂质;若氢气不足,Na会有剩余。
(4)丙同学是用测氢气体积的方法来测定NaH样品纯度的,甲装置会导致内部压强大于大气压强,丙装置无法测氢气的体积,丁装置与甲装置类似,会导致结果偏大,故选乙装置;若两次测得的氢气体积相同,则说明已冷却至室温。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是
A. “霾尘积聚难见路人”,霾尘所形成的气溶胶有丁达尔效应
B. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C. “青蒿一握,以水二升渍,绞取汁”,此法对青蒿素的提取属于化学变化
D. 古剑“沈卢”“以剂钢为刃,柔铁为茎干”,剂钢指的是铁的合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化四磷是黄绿色针状结晶,其结构如图所示。不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机溶剂,在沸腾的NaOH稀溶液中会迅速水解。回答下列问题:
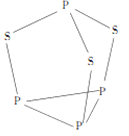
(1)Se是S的下一周期同主族元素,其核外电子排布式为____________。
(2)第一电离能:S______(填“>”、“<”或“=”,下同)P,电负性:S_____P。
(3)三硫化四磷分子中P原子采取_________杂化,与PO3-互为等电子体的化合物分子的化学式为_______。
(4)二硫化碳属于________(填“极性”或“非极性”)分子。
(5)用NA表示阿伏伽德罗常数的数值,0.1mol三硫化四磷分子中含有的孤电子对数为_________。
(6)叠氮酸(HN3)在常温下是一种液体,沸点较高,为308.8K,主要原因是_____________。
(7)氢氧化钠具有NaCl型结构,其晶胞中Na+与OH-之间的距离为αcm,晶胞中Na+的配位数为______,用NA表示阿伏加德罗常数的数值,NaOH的密度为_______g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 1.8g18O2分子与1.8g18O3分子中含有的中子数不同
B. 7.8gNa2S和7.8g Na2O2中含有的阴离子数目均为0.1NA
C. 23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元
D. 含16 g氧原子的二氧化硅晶体中含有的δ键数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种常用的植物调味油,可按如下路线合成:

已知:![]()
回答下列问题:
(1)下列关于乙烯的说法不正确的是_________(填字母)。
a.分子中所有原子共平面
b.能发生氧化反应,不能发生还原反应
c.能发生加聚反应生成高分子
d.能使酸性高锰酸钾溶液褪色
(2)由F生成G的反应类型为_________________________。
(3)C中官能团的名称为___________,由C生成D的反应类型为___________。
(4)D的化学名称为___________,由D生成E的化学方程式为___________。
(5)苯环上含有两个取代基,且分子中含有酯基的F的同分异构体有_________种,其中核磁共振氢谱显示有四组峰,且峰面积之比为3:2:2:3的是__________(填结构简式)。
(6)参照上述合成路线,设计以B为原料(无极试剂任选)制备高吸水性树脂![]() 的合成路线:________________。
的合成路线:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用浓盐酸与二氧化锰在加热的条件下反应生成二氯化锰与氯气,纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如图,回答下列问题:
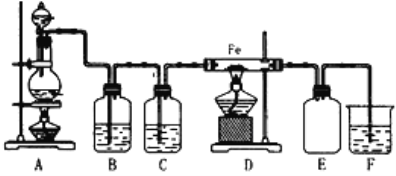
(1)A装置可制取氯气,反应前分液漏斗中药品为__.
(2)写出A装置中制取氯气所发生的化学方程式是__.
(3)装置B中盛放的试剂是__.
(4)装置E的作用是__.
(5)装置C的作用是__.
(6)装置F中发生反应的化学方程式是__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不涉及化学变化的是
A. 铁粉作袋装食品的抗氧化剂 B. 二氧化硫作纸浆的漂白剂
C. 氢氟酸作普通玻璃的刻蚀剂 D. 利用渗析实验除去淀粉溶液中的NaC1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com