
����Ŀ��������Ԫ��W��X��Y��Z��ԭ��������������W��Y����������֮��ΪX��������������2����Z�����������������ڲ��������X��Y��Z�ļ����ӵĵ��Ӳ�ṹ��ͬ��W�ĵ����ǿ��������������������塣����˵����ȷ����
A. Y�����������Գ�ˮ��������Ա�W��ǿ
B. W����̬�⻯���X���ȶ�
C. ���Ӱ뾶�Ĵ�С˳��r(w)>r(X)>r(Y)>(Z)
D. XY2��ZY2�еĻ�ѧ��������ͬ
���𰸡�C
�����������������������Ԫ��W��X��Y��Z ��ԭ��������������W�ĵ����ǿ�������������������壬��WΪNԪ�أ�Z�����������������ڲ��������ԭ����������NԪ�أ�ֻ�ܴ��ڵ������ڣ���ZΪMgԪ�أ�X��Y��Z�ļ����ӵĵ��Ӳ�ṹ��ͬ���ṹԭ��������֪��Xֻ�ܴ��ڵڶ����ڣ�����������������5��W(��Ԫ��)��Y����������֮��ΪX��������������2������Yԭ������������ֻ��Ϊ���������ԭ��������֪��Y�����ܴ�����A�壬ֻ�ܴ�����A�壬��YΪFԪ�أ�X����������Ϊ![]() =6����XΪOԪ�ء�A��ZΪMgԪ����������ϼ�Ϊ+2��YΪFԪ�أ�û����������ϼۣ���A����B���ǽ�����O��N�����⻯���ȶ���H2O��NH3����B����C��������ͬ���Ӳ�ṹ�����ӣ��˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶r(N3-)��r(O2-)��r(F-)��r(Mg2+)����C��ȷ��D��OF2�к��й��ۼ���MgF2�к������Ӽ�������ѧ�����Ͳ�ͬ����D����ѡC��
=6����XΪOԪ�ء�A��ZΪMgԪ����������ϼ�Ϊ+2��YΪFԪ�أ�û����������ϼۣ���A����B���ǽ�����O��N�����⻯���ȶ���H2O��NH3����B����C��������ͬ���Ӳ�ṹ�����ӣ��˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶r(N3-)��r(O2-)��r(F-)��r(Mg2+)����C��ȷ��D��OF2�к��й��ۼ���MgF2�к������Ӽ�������ѧ�����Ͳ�ͬ����D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ����Fe3+��Mg2+��Fe2+��Al3+�������ӣ��������м������������������Һ���Ȳ���ֽ��裬�ټ���������ᣬ��Һ�д������ٵ���������
A��Fe3+ B��Mg2+ C��Fe2+ D��Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015������ר�����Ƴ�����һ��������ɳ��ij������������ӵ�أ��ֱ��Խ�������ʯīΪ�缫����A1C14-��A12C17-���л���������ɵ������Һ����ŵ繤��ԭ������ͼ��ʾ������˵������ȷ���ǣ� ��
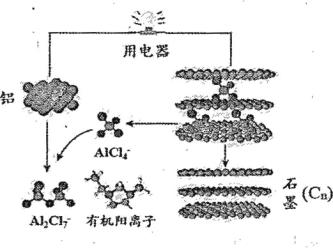
A���ŵ�ʱ����Ϊ������ʯīΪ����
B�����ʱ��������ӦΪ��Cn+ A1C14- - e-= Cn A1C14
C������ʱ�ĸ�����ӦΪ:Al-3e- +7 A1C14-=4A12C17-
D���ŵ�ʱ���л������������缫�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѣ�CH3OCH3������Ϊ21���͵�������Դ������ࡢ��Ч�����������Ļ���������
I����ҵ�Ʊ������ѵ������������£�

����Ӧ���У�ѹ��2.0��10.0Mpa���¶�230��280�棩�������·�Ӧ��
CO��g��+2H2��g��![]() CH3OH��g����H=-90.7kJ/mol ��
CH3OH��g����H=-90.7kJ/mol ��
2CH3OH��g��![]() CH3OCH3��g��+H2O��g����H=-23.5kJ/mol ��
CH3OCH3��g��+H2O��g����H=-23.5kJ/mol ��
CO��g��+H2O��g��![]() CO2��g��+H2��g����H=-41.2kJ/mol ��
CO2��g��+H2��g����H=-41.2kJ/mol ��
��1�������������Ƶúϳ�������Ӧ���£�CH4(g)+![]() O2
O2![]() CO(g)+2H2(g) ��H=-35.6kJ/mol���÷�Ӧ��_______��Ӧ�������Է����������Է�����
CO(g)+2H2(g) ��H=-35.6kJ/mol���÷�Ӧ��_______��Ӧ�������Է����������Է�����
��2������Ӧ�����ܷ�Ӧ3CO��g��+3H2��g��![]() CH3OCH3��g��+CO2��g���ġ�H=______��830��ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K______1.0�����������������=������
CH3OCH3��g��+CO2��g���ġ�H=______��830��ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K______1.0�����������������=������
��3��������Ӧ�У�����ѭ��ʹ�õ�������________��
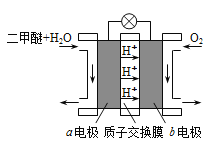
II����ͼΪ��ɫ��Դ��������ȼ�ϵ�����Ĺ���ԭ��ʾ��ͼ��b �缫��______����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶Ⱥ�ѹǿ�£�2���X2������3���Y2����ǡ����ȫ��Ӧ������2������廯����Z����Z�Ļ�ѧʽ������(����)
A��XY3 B��XY C��X3Y D��X2Y3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(N2H4)�Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��ش��������⣺
(1)N2H4��Nԭ�Ӻ��������ﵽ8�����ȶ��ṹ��д��N2H4�Ľṹʽ��___________��
(2)ʵ���������ֹ�����ȡNH3�ķ�Ӧ��ѧ����ʽΪ_____________��
(3)NH3��NaClO��Ӧ�ɵõ���(N2H4)���÷�Ӧ�Ļ�ѧ����ʽΪ_____________��
(4)��һ����ȼ�ϵ����һ�ּ��Ի�����أ��õ�طŵ�ʱ�������ķ�ӦʽΪ_____________��
(5)��ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]��Ӧ�Ļ�ѧ����ʽΪ2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
T/�� | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
���ʱ��H_________0(���������������=��)��
����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮��(��̼��)\frac{n(NH_{3})}{n(CO_{2})}=x����ͼ�ǰ�̼��(x)��CO2ƽ��ת����(��)�Ĺ�ϵ��������x����������ԭ����_____________��ͼ��A�㴦��NH3��ƽ��ת����Ϊ___________��
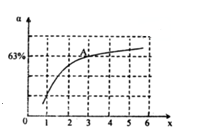
(6)�ں��º����ܱ������а��ռס��ҡ������ַ�ʽ�ֱ�Ͷ�ϣ�������Ӧ��N2(g)+3H2(g)2NH3(g)����ü�������H2��ƽ��ת����Ϊ40%��
n(N2) | n(H2) | n(NH3) | |
�� | 1mol | 3mol | 0mol |
�� | 0.5mol | 1.5mol | 1mol |
�� | 0mol | 0mol | 4mol |
���ж��������з�Ӧ���еķ�����_____________(����������)�ƶ���
�ڴ�ƽ��ʱ���ס��ҡ�����������NH3�����������С˳��Ϊ_____________��
��6�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����д���÷�Ӧ�Ļ�ѧ����ʽ�� ����ѧ�����ô�ԭ������Ƴɰ���һ����ȼ�ϵ�أ���ͨ�백���ĵ缫��
��7��һ�������£�ij�ܱ������з�����Ӧ��4NH3��g��+5O2��g��![]() 4NO��g��+6H2O��g������һ��������ܱ������У�Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ������д�ʩ�пɲ��õ��� ������ĸ���ţ���
4NO��g��+6H2O��g������һ��������ܱ������У�Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ������д�ʩ�пɲ��õ��� ������ĸ���ţ���
a������ѹǿ b���ʵ������¶� c������O2��Ũ�� d��ѡ���Ч����
��8�����ij��ˮ�ĵ���̶�Ϊ1%��Ũ��Ϊ0.01 mol/LMgCl2��Һ�μ���ˮ����ʼ��������ʱ(��������Һ����仯)����Һ�е�NH3��H2O��Ũ��Ϊ {��֪Ksp[Mg(OH)2]=4.0��10-12]}
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������
A������������ˮ��Ӧ��ȡ��������
B����������������������
C����������������ɫ����
D����������ʢװ�ռ���Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ĵ�С�����������ؼ����ص��ǣ� ��
A�����Ӹ��� B������ֱ�� C��ѹǿ D���¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1mol X��1mol Y�����2 L���ܱ����������������·�Ӧ 2X(g)��Y(g) =nZ(g)
��2W(g)��2minĩX�����ʵ���Ϊ0.2mol����Z��Ũ�ȱ�ʾ�ķ�Ӧ����Ϊ0.1mol/��L��min��
��ش���
��1��ǰ2min��X��Ũ�ȱ�ʾ��ƽ����Ӧ����
��2��nֵ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com