
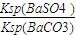 =4.4×10-2;故C正确;
=4.4×10-2;故C正确;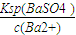 =
=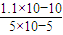 =2.2×10-6 mol?L-1;故D正确;
=2.2×10-6 mol?L-1;故D正确;

科目:高中化学 来源: 题型:
 2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为
2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 电离常数 |
| HClO | Ka=3×10-8 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
在1青团L含0.001 mol·L-1 SO![]() 的溶液中,注入0.01 mol·L-1BaCl2,能否使SO
的溶液中,注入0.01 mol·L-1BaCl2,能否使SO![]() 沉淀完全?〔已知Ksp(BaSO4)=1.08×10-10〕
沉淀完全?〔已知Ksp(BaSO4)=1.08×10-10〕
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com