
 2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为
2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为 2C(g),结合C的物质的量的变化量△n(C),计算出△n(A),再利用n(A)初始=n(A)平衡+△n(A);
2C(g),结合C的物质的量的变化量△n(C),计算出△n(A),再利用n(A)初始=n(A)平衡+△n(A);| [c(C)]2 |
| c(C)[c(B)]3 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1mol |
| 2L |
| 0.4mol |
| 2L |
| 0.4mol |
| 2L |
| [c(C)]2 |
| c(C)[c(B)]3 |
| (0.2mol/L)2 |
| 0.5mol/L×(0.2mol/L)3 |
| 2.8mol |
| 4L |
| 0.4mol |
| 4L |
| 0.4mol |
| 4L |
| (0.1mol/L)2 |
| 0.7mol/L×(0.1mol/L)3 |
| 1×10-10 |
| Ksp(BaCO3) |
| c(Ba2+) |
| 5×10-9 |
| 10-5 |
| KW |
| Ka |
| 10-14 |
| 10-6 |


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
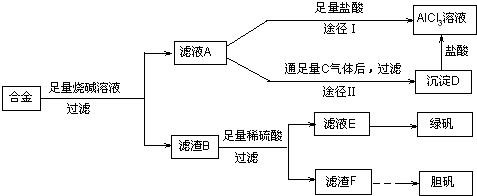


查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖南省衡阳市祁东三中高三(上)第三次周考化学试卷(解析版) 题型:填空题
 2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为 mol,平衡常数K= ,恒温恒压时,再向此容器内通入1.8mol A,平衡将 (填“正向”、“逆向”或“不”)移动.
2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为 mol,平衡常数K= ,恒温恒压时,再向此容器内通入1.8mol A,平衡将 (填“正向”、“逆向”或“不”)移动.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com