
【题目】绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
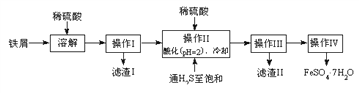
查询资料,得有关物质的数据如下表:
25℃时 | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 |
pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为____________________。
A.KSCN溶液B.NaOH溶液C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是(写两点)___________、____________。
(3)操作IV的顺序依次为________、冷却结晶、过滤。
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取3.72g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为_________(填仪器名称)。
②计算上述样品中FeSO47H2O的质量分数为__________。
③上述测定中,若滴定管规格为50mL,则步骤a中称取样品的质量不能超过______g。(保留4位小数)
【答案】 A 除去溶液中的Sn2+离子 将Fe3+还原成Fe2+ 蒸发浓缩 酸式滴定管 75% 9.3000
【解析】(1)检验所得绿矾晶体中是否含有Fe3+的实验操作是利用三价铁离子检验方法:,Fe3+和SCN-会反应生成红色的Fe(SCN)3,从而证明了Fe3+的存在。所以答案为A选项。
(2)通入硫化氢至饱和的目的是:硫化氢具有强还原性,可以将Fe3+还原为Fe2+。将H2S在溶液中饱和,可以增大溶液中的S2-浓度,尽量保证将Sn2+转化为SnS沉淀,以便于过滤除去Sn杂质。故答案为:除去溶液中的Sn2+离子,并将Fe3+还原成Fe2+。
(3)溶液中得到晶体,需要对溶液进行加热蒸发浓缩,冷却结晶,过滤,洗涤,干燥等,所以操作IV的顺序依次为:蒸发浓缩,冷却结晶,过滤。故答案为:蒸发浓缩。
(4)①高锰酸钾溶液具有强氧化性,所以会氧化碱式滴定管尖嘴处的橡胶管,所以滴定时盛放KMnO4溶液的仪器为酸式滴定管。
②用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL,则根据方程式:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O得到:n(Fe2+)=0.01000mol/L×0.0200L×5=0.001mol。所以250mL溶液中有n(Fe2+)=0.01mol。则FeSO47H2O物质的量也是0.01mol,质量为0.01mol×278g/mol=2.78g,质量分数为:2.78g÷3.72g=![]() =74.73%=75%。
=74.73%=75%。
③若滴定管规格为50mL,则最多盛放50mL的高锰酸钾溶液,根据方程式:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O得到最多反应的n(Fe2+)=0.01000mol/L×0.0500L×5=0.0025mol,所以250mL溶液中有n(Fe2+)=0.025mol,则FeSO47H2O物质的量最多是0.025mol,质量为0.025mol×278g/mol=6.95g,因为样品中FeSO47H2O的质量分数为![]() ,所以样品质量为6.95÷
,所以样品质量为6.95÷![]() =9.3g,题目要求保留4位小数,所以为9.3000g。
=9.3g,题目要求保留4位小数,所以为9.3000g。


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】能用离子方程式 2H+ + CO32-→CO2↑+H2O 表示的是
A.NaHSO4 和 Na2CO3B.HCl 和 BaCO3
C.CH3COOH 和 Na2CO3D.HI 和 NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知

A. X、Y、Z中最简单氢化物稳定性最弱的是Y
B. 元素氧化物对应水化物的酸性:Z>Y
C. 元素形成的单核阴离子还原性:X>Y
D. Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用氧化还原反应的有关知识回答下列问题.
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质.则在Cu、Fe、Ag中,的还原性最强;在Cu2+、Fe2+、Ag+中,的氧化性最强.
(2)在下列反应中:
A.2F2+2H2O═4HF+O2 B.2Na+2H2O═2NaOH+H2↑
C.CaO+H2O═Ca(OH)2 D.2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
①水只作还原剂的是
②水既不作氧化剂又不作还原剂的是 .
(3)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O. 取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4L.
MnCl2+Cl2↑+2H2O. 取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4L.
请回答下列问题:
①写出该反应的离子方程式 .
②该反应中,氧化剂是 , 氧化产物是 .
③反应中被氧化的HCl的物质的量为 .
④实验室备用的浓盐酸质量分数为36.5%,密度为1.19gcm﹣3 , 为使用方便,请计算出该浓盐酸中HCl的物质的量浓度 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 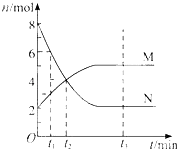
A.反应的化学方程式为:2MN
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是

A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7
B. 化合物F中含有共价键和离子键
C. 0.1molB与足量C完全反应共转移电子数为0.2NA
D. Z元素的最高正价为+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1H < 0(I)
NaNO3(s)+ClNO(g) K1H < 0(I)
2NO(g)+Cl2(g)![]() 2ClNO(g) K2H < 0(II)
2ClNO(g) K2H < 0(II)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______(用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=8.0×10-3molL-1min-1,回答下列问题
①平衡后n(Cl2)=__________mol,
②NO的转化率а1=_______。
③其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2________а1(填“>”“<”或“=”),平衡常数K2___________(填“增大”“减小”或“不变”)。
④若要使K2减小,可采用的措施是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物体的生命活动离不开水,下列关于水的叙述,错误的是( )
A. 在最基本生命系统中,H2O有自由水和结合水两种存在形式
B. 由氨基酸形成多肽链时,生成物H2O中的氢来自氨基和羧基
C. 有氧呼吸时,生成物H2O中的氢来自线粒体中丙酮酸的分解
D. H2O在光下分解,产生的[H]将固定的CO2还原成(CH2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com