
 (9)CH2=CH-CH3(8)
(9)CH2=CH-CH3(8) (10)
(10) (11)2,2-二甲基丁烷
(11)2,2-二甲基丁烷 和(8)
和(8) 是同一物质,
是同一物质, 分子式相同,但结构不同,故互为同分异构体,
分子式相同,但结构不同,故互为同分异构体, 和(11)2,2-二甲基丁烷结构相似,分子组成相差1个“CH2”原子团,故互为同系物,
和(11)2,2-二甲基丁烷结构相似,分子组成相差1个“CH2”原子团,故互为同系物, 和(11)2,2-二甲基丁烷结构相似,分子组成相差1个“CH2”原子团,故互为同系物,
和(11)2,2-二甲基丁烷结构相似,分子组成相差1个“CH2”原子团,故互为同系物,

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能.以葡萄糖溶液作底物为例,其工作原理如图所示.
微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能.以葡萄糖溶液作底物为例,其工作原理如图所示.| 序号 | A | B | C | D | E |
| 污水类型 | 生活污水 | 印染 | 电镀 | 造纸 | 硫酸工业废水 |
| COD值/mg?L-1 | 520 | 870 | 20 | 960 | 120 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 溶液中的盐 | 固体不溶物的成分 |
| ① | FeCl3、CuCl2 | Fe、Cu |
| ② | FeCl2、CuCl2 | Cu |
| ③ | FeCl2 | Cu |
| ④ | FeCl3、CuCl2 | Cu |
| ⑤ | FeCl2、CuCl2 | Fe |
| ⑥ | FeCl2、CuCl2、FeCl3 | 没有固体不溶物 |
| ⑦ | FeCl2 | Fe、Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| BaSO4(BaCO3) | ||
| FeSO4(CuSO4) | ||
| NaCl(HCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
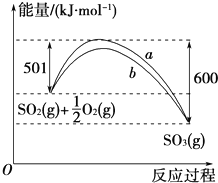 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相对分子质量相同,必定同一种物质或同分异构体 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有乙醇生成 |
| C、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| D、分子式相差一个或若干个“CH2”的有机物必定属于同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com