
【题目】某化学小组试利用废铝屑(含杂质铁)制备硫酸铝晶体,并对硫酸铝晶体进行热重分析,其主要实验流程如图1: 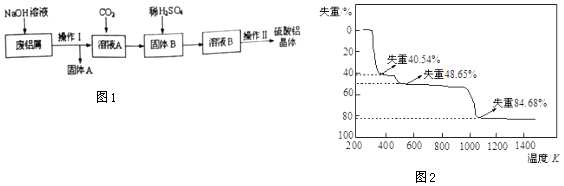
(1)向溶液A中通入过量的CO2 , 发生反应的离子方程式为 .
(2)操作II所包含的实验操作的名称依次为、冷却结晶、、洗涤、干燥.
(3)若开始时称取的废铝屑的质跫为5.00g,得到固体A的质量为0.95g,硫酸铝晶体的质量为49.95g(假设每一步的转化率均为100%),则所得硫酸铝晶体的化学式为 .
(4)取以上制得的硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:第一阶段失重40.54%,第二阶段失重48.65%,第三阶段失重84.68%,以后不再失重.其热分解的曲线如图2所示. 已知:失重%= ![]() ×100%
×100%
①失重第一阶段反应的化学方程式为 .
②失重第三阶段残留固体的化学式为 .
【答案】
(1)2Al+2NaOH+2H2O═2NaAlO2+3H2↑
(2)蒸发浓缩;过滤
(3)Al2(SO4)3·18H2O
(4)Al2(SO4)3.18H2O ![]() Al2(SO4)3.3H2O+15H2O; Al2(SO4)3
Al2(SO4)3.3H2O+15H2O; Al2(SO4)3![]() Al2O3+3SO3↑
Al2O3+3SO3↑
【解析】解:(1)Al和氢氧化钠溶液生成可溶性的偏铝酸钠与氢气,镁不反应,反应方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;(2)从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作;
故答案为:蒸发浓缩;过滤;(3)Al的质量为5g﹣0.95g=4.05g,其物质的量为4.05g÷27g/mol=0.15mol,设硫酸铝晶体化学式为:Al2(SO4)3·nH2O,根据Al元素守恒,硫酸铝晶体的物质的量为0.15mol÷2=0.075mol,故硫酸铝晶体的相对分子质量为49.95÷0.075=666,则54+96×3+18n=666,解得n=18,故该硫酸铝晶体的化学式为:Al2(SO4)3·18H2O;
故答案为:Al2(SO4)3.18H2O;(4)晶体中结晶水的含量为 ![]() =48.65%,故第二阶段完全失去结晶水,得到物质为Al2(SO4)3,第一阶段失去部分结晶水,失去结晶水数目为
=48.65%,故第二阶段完全失去结晶水,得到物质为Al2(SO4)3,第一阶段失去部分结晶水,失去结晶水数目为 ![]() =15,故第一阶段得到的物质为Al2(SO4)3·3H2O,反应方程式为:Al2(SO4)3·18H2O
=15,故第一阶段得到的物质为Al2(SO4)3·3H2O,反应方程式为:Al2(SO4)3·18H2O ![]() Al2(SO4)3·3H2O+15H2O;
Al2(SO4)3·3H2O+15H2O;
第三阶段剩余物质的相对分子质量为666×(1﹣84.68%)=102,应是Al2O3,故硫酸铝反应生成氧化铝与三氧化硫,反应方程式为:Al2(SO4)3 ![]() Al2O3+3SO3↑;
Al2O3+3SO3↑;
故答案为:Al2(SO4)3.18H2O ![]() Al2(SO4)3.3H2O+15H2O;Al2(SO4)3
Al2(SO4)3.3H2O+15H2O;Al2(SO4)3 ![]() Al2O3+3SO3↑.
Al2O3+3SO3↑.
向废铝屑(含杂质铁)中加入足量氢氧化钠溶液,发生反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,铁不反应,固体A为Fe,采用过滤的方法进行分离,溶液A为NaAlO2溶液,向其中通入二氧化碳,发生反应:NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3,再通过过滤进行分离,固体B为氢氧化铝,氢氧化铝与硫酸反应得到硫酸铝溶液,再经过蒸发浓缩、冷却结晶、洗涤、干燥得到硫酸铝晶体;(1)Al和氢氧化钠溶液生成可溶性的偏铝酸钠;(2)从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作;(3)Al的质量为5g﹣0.95g=4.05g,设硫酸铝晶体化学式为:Al2(SO4)3·nH2O,根据Al元素守恒计算硫酸铝晶体的物质的量,再计算硫酸铝晶体的相对分子质量,进而计算n的值,确定化学式;(4)根据(3)中计算可知,晶体中结晶水的质量分数,低温加热,首先失去结晶水,高温下,最终硫酸铝分解,根据失重计算判断各阶段分解产物,再书写化学方程式.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示. 
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣.此时,应向污水中加入适量的 .
A.BaSO4
B.CH3CH2OH
C.Na2SO4
D.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是 Ⅰ.;
Ⅱ. .
(3)电极反应I和Ⅱ的生成物反应得到Fe(OH3)沉淀的离子方程式是 .
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极.为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图).A物质的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为阳离子交换膜法以石墨为电极电解饱和食盐水原理示意图.据图判断下列说法不正确的是( ) 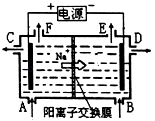
A.标准状况下,生成22.4LCl2的同时有2molNaOH生成
B.从C口流出的是NaOH溶液
C.从E口逸出的气体是H2
D.从F口逸出的气体是Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( ) 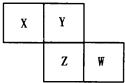
A.Z的单质与氢气反应较Y剧烈
B.X、Y形成的化合物都易溶于水
C.只由这四种元素不能组成有机化合物
D.最高价氧化物对应水化物的酸性W比Z弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学的发展、社会的进步和生活水平的提高都离不开化学的发展和各种材料的开发制造.
(1)中国高铁发展迅速,高铁建设使用的主要材料有钢铁、铝合金和玻璃等.
①高炉炼铁和制造普通玻璃都要用到的原料是 . 高温下将铁矿石还原为金属铁的主要还原剂是 .
②下列关于铝及铝合金的叙述不正确的是(填字母).
a.密度小 b.抗腐蚀能力强 c.不与浓硫酸反应
③钢铁、铝合金、玻璃都属于(填字母).
a.混合物 b.化合物 c.单质
(2)化学实验和科学研究中,经常需要配制一定物质的量浓度的溶液.欲配制0.2mol/LNa2CO3溶液100mL.
①容量瓶在使用前首先应该 . 需要用托盘天平称量Na2CO3的质量为g.
②配制时,需“将容量瓶塞盖好,反复上下颠倒,摇匀”,摇匀前的一步操作是 .
③下列操作,会使最后配成溶液的实际浓度比所要求的浓度偏小的是(填字母).
a.定容时,俯视刻度线,溶液的凹面和刻度线相切,停止加水
b.定容时,如果加水超过了刻度线,立即用胶头滴管吸出多余的部分
c.将称出的Na2CO3在烧杯中溶解,所得溶液恢复至室温再转移到容量瓶中
④准确量取一定体积所配制的Na2CO3溶液加少量水稀释,则稀释前后的溶液分别与盐酸反应时,消耗HCl的物质的量(填“相同”、“不相同”、或“无法确定”).
(3)生活环境的改善,需要对生活和生产中的废弃进行处理.
①燃煤排放的二氧化硫会被雨水吸收形成酸雨,这种酸雨在空气中放置酸性增强的原因是(用化学方程式表示).可以在已酸化的土壤中撒些从而消除酸雨造成的影响.
②氮肥和硝酸的工业生产以及汽车等交通工具的使用,会有大量的氮氧化物排放到空气中,这些氮氧化物对环境造成的影响有(填一种即可).氮氧化物可用氢氧化钠溶液吸收转化为NaNO3、和H2O.汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳转化为CO2和 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的一些常见物质之间的转化关系中(有些反应中的水、部分产物及反应条件未列出),已知反应①是工业制硫酸时沸腾炉中的反应,A是由两种元素组成的化合物且元素的质量比为7:8,B、M为非金属单质,E、K为金属单质,其中B为地壳中含量最多的非金属元素的单质,E为地壳中含量最多的金属元素的单质. 
(1)反应②的一种用途为 .
(2)M的化学式为 .
(3)反应①的化学方程式为 .
(4)I的水溶液与K反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活、环境保护、资源利用等密切相关,下列说法正确的是
A.大米、玉米、小麦中的淀粉经水解可变成乙醇
B.棉花、蚕丝和人造丝的主要成分都是纤维素
C.利用二氧化碳制造全降解塑料,可以缓解温室效应
D.海洋中含有丰富的矿产资源,仅利用物理方法就可以获得NaCl、Br2和Mg等物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题. 
(1)D元素原子的结构示意图为;
(2)A、B、C三种元素的原子半径由小到大的顺序为(用元素符号表示);
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈(填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为(用具体离子符号表示);
(5)实验室中,应将X的浓溶液保存在棕色试剂瓶中,其原因是(用化学方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72﹣(橙色)+H2O2CrO42﹣(黄色)+2H+ . 用K2Cr2O7溶液进行下列实验: 
结合实验,下列说法不正确的是( )
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72﹣被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com