

 、G的结构式为O=C=O;若向M溶液通入G否(是或否)有沉淀,若再通入足量E观察到的现象是有白色沉淀.
、G的结构式为O=C=O;若向M溶液通入G否(是或否)有沉淀,若再通入足量E观察到的现象是有白色沉淀.分析 B是浓溶液,海水去除氯化钠之后变为淡水,所以B是NaCl浓溶液,G是温室气体,则G为CO2,反应②在高温、高压、催化剂的条件下进行,应为工业合成氨的反应,根据各物质的转化关系,反应③应为候氏制碱法,所以X、Y为氮气和氢气,E为NH3,C分解能产生二氧化碳,则C应为碳酸氢钠,D为氯化铵,碳酸氢钠受热分解得二氧化碳、水、碳酸钠,A是无色液体,则A是水,所以N为碳酸钠,F高温分解生成二氧化碳,则F为碳酸钙,H为氧化钙,H与D的溶液反应生成M为氯化钙,据此答题.
解答 解:B是浓溶液,海水去除氯化钠之后变为淡水,所以B是NaCl浓溶液,G是温室气体,则G为CO2,反应②在高温、高压、催化剂的条件下进行,应为工业合成氨的反应,根据各物质的转化关系,反应③应为候氏制碱法,所以X、Y为氮气和氢气,E为NH3,C分解能产生二氧化碳,则C应为碳酸氢钠,D为氯化铵,碳酸氢钠受热分解得二氧化碳、水、碳酸钠,A是无色液体,则A是水,所以N为碳酸钠,F高温分解生成二氧化碳,则F为碳酸钙,H为氧化钙,H与D的溶液反应生成M为氯化钙,
(1)海水资源的利用要实现①通常采用最常用的为蒸馏法和淡化膜法,
故答案为:蒸馏法;淡化膜法;
(2)根据上面的分析可知,E为NH3,E的电子式为 ,G为CO2,G的结构式为 O=C=O,M为氯化钙,若向M溶液通入CO2没有沉淀,若再通入足量NH3观察到的现象是有白色沉淀,
,G为CO2,G的结构式为 O=C=O,M为氯化钙,若向M溶液通入CO2没有沉淀,若再通入足量NH3观察到的现象是有白色沉淀,
故答案为: ;O=C=O;否;有白色沉淀;
;O=C=O;否;有白色沉淀;
(3)反应③的化学方程式为NaCl+NH3+CO2=NaHCO3+NH4Cl,反应④的化学方程式:2NaHCO3=CO2↑+Na2CO3+H2O,
故答案为:NaCl+NH3+CO2=NaHCO3+NH4Cl;2NaHCO3=CO2↑+Na2CO3+H2O.
点评 本题考查无机物的推断,题目难度不大,本题注意把握物质的分子构成特点以及典型的物理性质,常作为推断题的突破口,答题时注意体会.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如下:| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 504mL | B. | 168mL | C. | 336mL | D. | 224mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 试样中一定不含Al3+ | |
| C. | 试样与Na2CO3溶液一定不能大量共存 | |
| D. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 85g | B. | 79g | C. | 116g | D. | 58g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
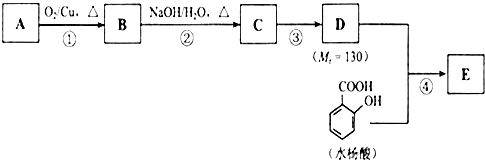
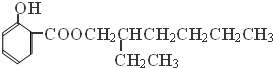 .
.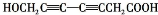 、
、 、
、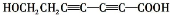 、
、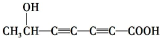 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 人们对苯的认识有一个不断深化的过程.
人们对苯的认识有一个不断深化的过程.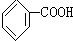 和生石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式:
和生石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式: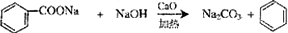 (NaOH参与反应)
(NaOH参与反应)
 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
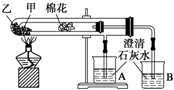
| A. | 甲为小苏打,乙为纯碱 | |
| B. | 要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 | |
| C. | 加热不久就能看到A烧杯的澄清石灰水变浑浊 | |
| D. | 整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com