
有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100mL,并向此稀稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的
 |
试分析NaOH在吸收CO2气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标况)是多少?
甲成分只能为NaOH和Na2CO3,且物质的量之比为1:1,产生CO2的体积为0.056L.
乙成分是Na2CO3和NaHCO3的混合物,由耗酸量可判断出物质之比为1:1,产生气体亦可由产生气体耗酸量求得,为0.112L。
NaOH溶液中通入一定量的CO2,有几种情况:一种情况是CO2不足,反应后的混合物为NaOH,Na2CO3;另一种情况是二者恰好完全反应生成Na2CO3;第三种情况是CO2过量,全部NaOH转化为NaHCO3;第四种情况是CO2过量,反应后的混合物为NaHCO3和Na2CO3。
分析甲图象:加入盐酸50mL时开始产生CO2气体,至反应完毕消耗25mL盐酸,根据反应:
Na2CO3+HCl=NaHCO3+NaCl ①
NaHCO3+HCl=NaCl+H??2O+CO2↑②
可知滴加到50mL时开始反应②,根据耗酸量可知NaHCO3的物质的量。分析图象加入50mL以前,无气体放出,与盐酸反应转化为NaHCO3应消耗25mL盐酸,则与NaOH反应的盐酸也应是25mL。由此得也甲成分只能为NaOH和Na2CO3,且物质的量之比为1:1,产生CO2的体积为0.056L.
分析乙图象:加入盐酸25mL时开始产生CO2气体,消耗50mL盐酸反应完全,耗酸为末产生气体时的2倍,说明原物质是Na2CO3和NaHCO3的混合物,由耗酸量可判断出物质之比为1:1,产生气体亦可由产生气体耗酸量求得,为0.112L。


科目:高中化学 来源: 题型:阅读理解
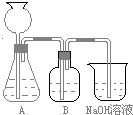
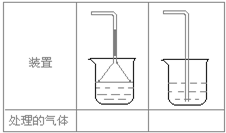
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
(1)最初加入的50mLNaOH溶液的作用是什么?
(2)计算所用硫酸的浓度。
(3)试判断两种氧化物各是什么。并计算其物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:038
将等物质的量的两种氧化物溶于100mL硫酸,而后逐滴加入1.00mol·L-1NaOH溶液,当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀随NaOH加入量逐渐增加。当NaOH的体积V2=650mL时,沉淀量达到最大值,继续滴加NaOH 时,沉淀量逐渐减小。当V3≥750mL时,沉淀量不再改变。
(1)最初加入的50mLNaOH溶液的作用是什么?
(2)计算所用硫酸的浓度。
(3)试判断两种氧化物各是什么。并计算其物质的量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com