
����Ŀ��һ�ֺ��ᾧˮ����ɫ����ɱ�ʾΪAnH2O�����нᾧˮ����������Ϊ28.57%���þ������ˮ��A��̼���⡢������Ԫ�ص����������ֱ�Ϊ26.67%��2.23%��71.1%��
�Իش��������⣺
��1������ˮ��A�����ʽ��
��2��A��NaOH��Һ�����кͷ�Ӧ��������ʽ�κ�һ�����Σ�0.9g��ˮ��Aǡ�ú�0.1molL��1NaOH��Һ200mL��ȫ��Ӧ�������Σ���û�����A�ķ���ʽ����ṹ��ʽ������ʾ����COOH��һ�����Թ����ţ�����д��������A������NaOH��Ӧ�Ļ�ѧ����ʽ
��3����AnH2O��n��ֵ��
���𰸡�
��1��CHO2
��2��HOOC��COOH+2NaOH=Na2C2O4+2H2O
��3��
�⣺ ![]() ����� n=2
����� n=2
��AnH2O��n��ֵΪ2��
���������⣺��1��������ԭ�Ӹ�����ΪN��C����N��H����N��O��= ![]() ��
�� ![]() ��
�� ![]() =1��1��2��
=1��1��2��
������ˮ��B�����ʽΪ CHO2
���Դ��ǣ�CHO2����2��B��NaOH��Һ�����кͷ�Ӧʱ��������һ����ʽ�κ����Σ�˵��BΪ��Ԫ�ᣮ
������
B | + | 2NaOH | �T | Na2B + | H2O |
Mrg | 2mol | ||||
0.15g | 0.1��0.0334mol |
���� Mr=90
��B�ķ���ʽ��CHO2��m��
���� ![]()
����B�ķ���ʽΪ��C2H2O4 �� �ṹ��ʽΪHOOC��COOH��
���������Ʒ�Ӧ�ķ���ʽΪHOOC��COOH+2NaOH=Na2C2O4+2H2O��
���Դ��ǣ�C2H2O4��HOOC��COOH��HOOC��COOH+2NaOH=Na2C2O4+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ�ó��Ľ��۴������( )
A.ά��������ϳ����أ�ͻ�����������л���Ľ���
B.�Ž��з���ǰ�˹����Ļ������ܽ����Ԫ�������ɣ�������ѧ�о���Ҫ�̳���Ҫ����
C.C60��Ӣ����������ѧ�ҹ�ͬ���ֵģ������˹��ʿƼ���������Ҫ��
D.�ƶ��Ͳ��ն������ۻ�ѧ����Ĺ���ŵ������ѧ������ζ�Ż�ѧ�ѳ�Ϊ�������о�Ϊ����ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�����������ԭ��Ӧ�����������������
A.K+��H+��I-��MnO4-B.Fe3+��Fe2+��SO42-��NO3-
C.Al3+��Na+��SO42-��CO32-D.Fe3+��H+��SO42-��ClO-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺ 
��1���ؿ��к�����ߵĽ���Ԫ�������ڱ��е�λ���� ��
��2�����γɵĵ�����ˮ��Ӧ�����ӷ���Ϊ ��
��3���ڢߵķǽ�����ǿ����ͨ���Ƚ�������Ԫ�������ţ�
a��ԭ�ӵĵõ��ӵ����� b�������������
c����̬�⻯����ȶ��� d�����ʵ��۷е�
��4��д��һ���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ������ʵĵ���ʽ ��
��5��������ҵ����ϳ�����Ԫ�آں͢��γɵĻ������Ӳ�ȱȽ��ʯ�����������γɵľ��廹���ܾ��е����ʻ��ص��������ţ�
���۵�ܸ� �ڿ��Ե��� �۲����ڵ������� �ܾ��пռ���״�ṹ
��6���ٺ͢��γɵ�ijҺ̬������Ħ��������������ͬ���ڳ��³�ѹ��0.25mol��Һ̬��������������������ȫȼ�����ɢ۵���̬���ʺ�Һ̬ˮ��ͬʱ�ų�QkJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڱ���˵������ȷ����( )
A. �����Է���ȡ����Ӧ
B. ���и�ԭ�Ӿ���ͬһƽ��
C. ����û�е��͵�̼̼˫��,���Բ��ܷ����ӳɷ�Ӧ
D. ���еĺ�̼����,ȼ��ʱ���������ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊԭ������ȼ���Ҵ����������̿�����ͼ��ʾ��
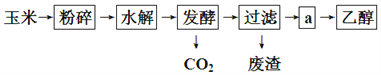
��1���Ҵ������������Ĺ����ŵ�����Ϊ��__________________��
��2�����˺�õ�a����Ҫ�ɷ�Ϊ�����Ǻ��Ҵ�������a�IJ�����__________��
A������ B����ȡ C������ D����Һ
��3������������Ϊ�˼���ˮ���Ƿ�ʼ����ʹ�õ��Լ���______________��
��4����֪1g�Ҵ���ȫȼ�շų�������Ϊ29.7kJ����ݴ�д���Ҵ�ȼ�յ��Ȼ�ѧ����ʽ��_______��
��5��Ϊ�˳�������Ҵ�����������ѧ�һ����Ҵ���Ƴ�ȼ�ϵ�أ���ͼ���û����������ܼ����ڸ��¹���ʱ���Ҵ����Ч�ʸ��Ҹ���ȫ�����жϣ��õ�ص�a��Ϊ��ص�_______�����������������b���ĵ缫��ӦʽΪ��____________________________����ع���ʱ������1mol�Ҵ�����������ת�Ƶĵ���Ϊ____________mol��
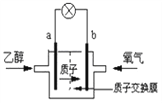
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������볣��Σ�ջ�ѧƷ�ķ����Ӧ����( )
A. Na������ʪ��ȼ��Ʒ B. Na2O2����������
C. Ũ���������ױ�Ʒ D. KOH������ʴƷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����25 ��ʱ��KW��1.0��10��14��ij�¶���Kw��1.0��10��12����˵���� ��
A. ij�¶ȱȳ���Ҫ�� B. ǰ�ߵ�c(H��)�Ϻ��ߴ�
C. ˮ�ĵ��������һ�����ȹ��� D. ij�¶��£�pH=7ʱ����Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�������������ȵ��ǣ� ��
A.10g H2��10g O2
B.5.6g N2 ����״������ 11g CO2
C.9g H2O ��0.5mol Br2
D.224mL H2����״������0.1mol N2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com