
| A. | 五种元素中B元素的金属性最强 | |
| B. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| C. | 元素C、D、E的最高价氧化物对应水化物的酸性递减 | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
分析 五种短周期主族元素A、B、C、D、E的原子序数依次递增,A2属于绿色燃料,则A为H元素;C的氧化物常用于玻璃的生产,则C为Si元素;D元素原子的核电荷数是同主族上一周期元素的2倍,则D为S元素;E的原子序数大于S,则E为Cl元素;B、C为同周期元素,则B位于第三周期,B、D原子最外层电子数之和等于E的最外层电子数,则B最外层电子数=7-6=1,为Na元素,据此结合元素周期律知识解答.
解答 解:五种短周期主族元素A、B、C、D、E的原子序数依次递增,A2属于绿色燃料,则A为H元素;C的氧化物常用于玻璃的生产,则C为Si元素;D元素原子的核电荷数是同主族上一周期元素的2倍,则D为S元素;E的原子序数大于S,则E为Cl元素;B、C为同周期元素,则B位于第三周期,B、D原子最外层电子数之和等于E的最外层电子数,则B最外层电子数=7-6=1,为Na元素,
A.五种元素中,Na(B)位于ⅠA族,其金属性最强,故A正确;
B.元素D、E分别S、Cl,非金属性:Cl>S,则对应氢化物的稳定性:A2D<AE,故B错误;
C.元素C、D、E分别为Si、S、Cl,非金属性逐渐增强,则最高价氧化物对应水化物的酸性逐渐增强,故C错误;
D.离子的电子层越多,离子半径越大,电子层相同时核电荷数越大,离子半径越小,则离子半径大小为:D>E>B,故D错误;
故选A.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水、酸性高锰酸钾溶液褪色的本质是不同的 | |
| B. | 淀粉、蛋白质、油脂都属于天然高分子化合物 | |
| C. | 聚氯乙烯塑料最适合用来做蔬菜、水果及熟食等的保鲜膜 | |
| D. | 等物质的量的CH4与Cl2恰好反应时,生成CH3Cl与HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
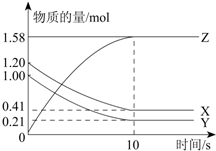
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨作电极电解CuSO4溶液,通电一段时间后,在标准状况下两极产生的气体可能相等 | |
| B. | 船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 电解池中的阳极和原电池中的负极上都发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符号为${\;}_8^{18}$O的原子常用于文物年代的测定 | |
| B. | 原子结构示意图 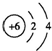 既可以表示12C,也可以表示14C 既可以表示12C,也可以表示14C | |
| C. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S2- | |
| D. | “84消毒液”中有效成分NaClO的电子式为  |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
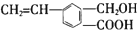 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | 分子式为C10H12O3 | |
| B. | 1 molNa2CO3,最多能消耗l mol有机物M | |
| C. | 1 molM与足量金属钠反应生成11.2 L气体(标准状况) | |
| D. | M能发生取代反应、氧化反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com