
| A、在盛有苯的试管中加入几滴酸性KMnO4溶液,可观察到紫色褪去 |
| B、向鸡蛋清溶液中滴加饱和CuSO4溶液,有固体析出,再加入足量蒸馏水,固体可以重新溶解 |
| C、用灯光照射盛有CH4与Cl2(体积比1:4)的集气瓶后,可观察到瓶内壁附有液态物质 |
| D、将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变黑,反复多次,并能闻到香味 |


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:
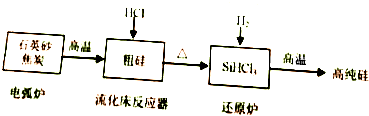 硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中有广泛应用,回答下列问题:
硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中有广泛应用,回答下列问题:| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
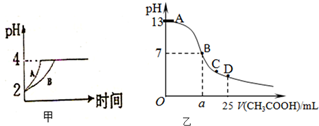 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.15 mol?L-1 |
| B、0.30 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| B、铜片加入氯化铁溶液中发生反应:3Cu+2Fe3+=3Cu2++2Fe |
| C、FeCl2、Fe(OH)3、Cu2S均可通过化合反应制得 |
| D、在pH=1溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、食品保鲜膜成分为聚氯乙烯 |
| B、甲醛可作为海产品的防腐剂 |
| C、盐析可提纯蛋白质并保持其生理活性 |
| D、医疗上用于消毒的酒精其体积分数为95% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、简单离子半径:Y>Z>W>Q>X |
| B、W2Z2与X2Z反应中氧化剂与还原剂物质的量之比为1:2 |
| C、X能分别与Y、Z、W形成共价化合物 |
| D、Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验溶液中是否含有Fe2+的方法是先滴加氯水,再滴加KSCN溶液 |
| B、铅蓄电池放电时的负极反应式为:Pb02+4H2SO4+2e-═PbSO4+2H2O |
| C、Na2CO3溶液加水稀释后,恢复至原温度,溶液的pH和Kw均减小 |
| D、某电池的总反应为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,每生成1mol Na2Mn5O10转移电子数2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com