
| A、被氧化的物质是氧化剂 |
| B、可以利用酒精将碘水中的碘提取出来 |
| C、化合反应一定不是氧化还原反应 |
| D、铝抗腐蚀是外层氧化膜致密的缘故 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.03mol/L |
| D、0.04mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2AB(g)?A2(g)+B2(g)△H>0 |
| B、A2(g)+3B2(g)?2AB3(g)△H<0 |
| C、A(s)+B(g)?C(g)+D(g)△H>0 |
| D、2A(g)+B(g)?3C(g)+D(s)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、90ml | B、150ml |
| C、175ml | D、200ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
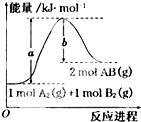
| A、每生成2分子AB吸收bkJ热量 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、断裂1molA-A和1molB-B键,放出akJ能量 |
| D、该反应热△H=+(a-b)kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com