
A、化合物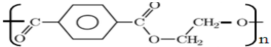 名称为聚对苯甲二酸乙二酯 名称为聚对苯甲二酸乙二酯 |
| B、C3H7OH与C4H9OH分子间脱水,最多可生成6种醚 |
C、1mol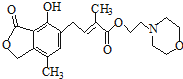 最多可与含4mol NaOH的水溶液完全反应 最多可与含4mol NaOH的水溶液完全反应 |
D、某油脂的化学式为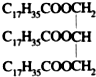 ,它属于酯类但不属于高分子化合物 ,它属于酯类但不属于高分子化合物 |
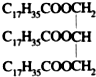 为高级脂肪酸甘油酯,属于油脂,相对分子量较小,不属于高分子化合物.
为高级脂肪酸甘油酯,属于油脂,相对分子量较小,不属于高分子化合物. 名称应该为:聚对苯二甲酸乙二酯,不是聚对苯二甲酸乙二酯,故A错误;
名称应该为:聚对苯二甲酸乙二酯,不是聚对苯二甲酸乙二酯,故A错误;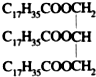 中含有酯基,属于酯类,由于油脂的相对分子量较小,不属于高分子化合物,故D正确;
中含有酯基,属于酯类,由于油脂的相对分子量较小,不属于高分子化合物,故D正确;

科目:高中化学 来源: 题型:
| A、稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | ||||
| B、铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | ||||
C、实验室制氯气:MnO2+4H++2Cl-
| ||||
| D、向氯化铝溶液滴加少量氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中含0.1NA个Fe(OH)3胶体粒 |
| B、标准状况下,11.2L C2H6含3NA个C-H极性共价键 |
| C、标准状况下,5.6L NO和5.6 L O2混合后的分子总数为0.5NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中增大,②中减小 |
| B、①中减小 ②中增大 |
| C、①、②中都增大 |
| D、①、②中都减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KH中H是-1价 |
| B、该反应转移的电子数为2个 |
| C、H2是氧化产物,也是还原产物 |
| D、KH可以在野外生存时做应急生氢药品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Cl-、SO42- |
| B、Na+、NO3-、CO32-、Cl- |
| C、Na+、H+、NO3-、SO42- |
| D、K+、NO3-、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com