
【题目】铬酸铅(PbCrO4)俗称铬黄,不溶于水。广泛用于涂料、油墨、漆布、塑料和文教用品等工业。实验室模拟工业上用铬污泥(含有Cr2O3、Fe2O3、Al2O3、SiO2等)制备铬黄的工艺流程如下:
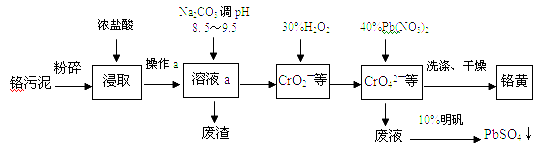
(1)铬黄中,铬的化合价为 价
(2)在浸取过程中浓盐酸与Fe2O3的离子方程式 ,操作a的名称为
(3)写出加入30%H2O2过程中发生的离子反应方程式
(4)在废液中加入10%明矾溶液发生反应的离子方程式为
(5)对含铬废水进行处理的方法是:将含Cr2O72-的酸性废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
①写出Fe2+和Cr2O72-发生反应的离子方程式
请分析电解过程中溶液pH不断上升的原因
【答案】(1)+6;(2)Fe2O3+6H+=2Fe3++3H2O;过滤;
(3)2CrO2—+3H2O2+2OH-=2CrO42-+4H2O;(4)SO42-+Pb2+=PbSO4↓;
(5)①6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
②电解时阴极消耗氢离子,亚铁离子还原Cr2O72-也消耗氢离子,所以pH不断上升。
【解析】
试题分析:(1)Pb以+2价稳定,根据铬酸铅的化学式,O为-2价,Pb为+2价,化合价代数和为0,因此Cr为+6价;(2)Fe2O3属于碱性氧化物,因此反应的离子反应方程式为Fe2O3+6H+=2Fe3++3H2O;操作a得到滤液和滤渣,因此操作名称为过滤;(3)利用过氧化氢的氧化性,把Cr3+氧化成+6价Cr,离子反应方程式为:2CrO2—+3H2O2+2OH-=2CrO42-+4H2O;(4)根据流程图,加入明矾的作用,发生SO42-+Pb2+=PbSO4↓;(5)①根据Cr2O72-的强氧化性,把Fe2+氧化成Fe3+,其离子反应方程式为:6Fe2+ + Cr2O72-+14H+ = 6Fe3+ + 2Cr3+ + 7H2O;②电解时阴极消耗氢离子,亚铁离子还原Cr2O72-也消耗氢离子,所以pH不断上升。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】已知牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生。某兴趣小组对摩擦剂成分及其含量进行以下探究:
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是______________。
(2)往(1)所得滤液中通入过量二氧化碳,主要发生反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
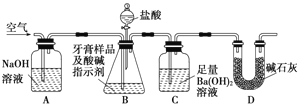
依据实验过程回答下列问题:
(3)D装置的作用是 ;
(4)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:______________。
(5)下列各项措施中,不能提高测定准确度的是________________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含淀粉、NaCl、Na2SO4、CaCl2的混合溶液,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
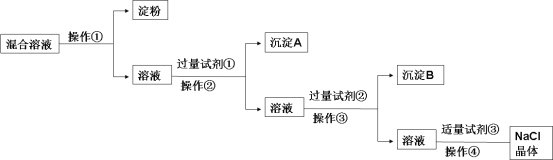
(1)操作①是利用胶体不能通过 而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:
试剂①___________________;试剂③_____________________。
(3)判断试剂①已过量的操作是:__________________。
(4)控制试剂③适量的方法是:__________________。
(5)试剂②的作用(用化学方程式表示):__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学变化属于加成反应的是
A.乙醇在铜作催化剂的条件下加热和空气的反应
B.乙烯通入溴的四氯化碳溶液中的反应
C.甲烷在光照条件下与氯气发生的反应
D.苯与液溴在铁粉作催化剂的条件下发生的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
①铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线拧在一起
②汽车尾气中含有能污染空气的氮氧化物,主要是汽油燃烧不充分造成的
③从海水中提取物质都必须通过化学反应才能实现
④“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料
⑤明矾可以用于净水,主要是由于Al3+水解生成的少量氢氧化铝胶体有净水作用
A.②③⑤ B.①②④ C.①③④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素:反应的方程式为:
CO(NH2)2+H2O2![]() CO(NH)2·H2O2。过氧化尿素的部分性质如下:
CO(NH)2·H2O2。过氧化尿素的部分性质如下:
合成过氧化尿素的流程及反应装置图如下:
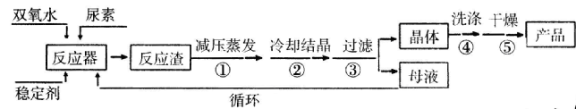
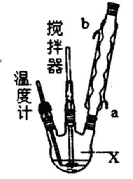
请回答下列问题:
(1)仪器X的名称是____________;冷凝管中冷却水从____________(填“a”或“b”)口进入。
(2)反应器的加热方式是_______________。
(3)搅拌器是否可用铁质材料___________(填“是”或“否”),原因是_______________。
(4)步骤① 采用减压蒸发的原因是___________。
(5)下列选项中,最适合作为步骤④ 的洗涤液是_______。
a.冰水 b.热水 c.饱和NaCl溶液 d.酒精和水的混合液
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol/L H2SO4,用0.1000 mol/L KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应)。
① 滴定终点的现象是______________。
② 则产品中CO(NH)2·H2O2的质量分数为______________。
③ 若滴定前仰视,滴定后俯视,则测得的过氧化尿素含量_________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验及显色结果的叙述,错误的是
A.水浴加热条件下,麦芽糖与斐林试剂发生反应生成砖红色沉淀
B.蛋白质溶液遇双缩脲试剂变紫色
C.人的口腔上皮细胞经健那绿染色后,可以看到呈蓝绿色的线粒体
D.常温条件下,脱氧核糖核酸与吡罗红作用呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含有Al2O3、SiO2和少量FeOxFe2O3的铝灰制备Al2(SO4)318H2O,工艺流程如下:
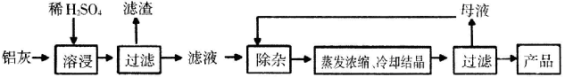
(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的PH

(1)H2SO4溶解Al2O3的离子方程式是____________。
(2)检验滤液中还存在Fe2+的方法是______________。
(3)“除杂”环节有如下几个步骤:(I)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2 (II)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤I 的目的是:_________;调节溶液的pH为3.2的目的是__________。
②向步骤II的沉淀中加入浓HCl并加热,有黄绿色气体生成,写出其反应方程式______。
③步骤Ⅲ中加入MnSO4的目的是__________(用离子反应方程式表示)
(4)从多次循环使用后母液中可回收的主要物质是________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化工生产的叙述中,符合目前工业生产实际的是( )
A.石油工业中,采用干馏的方法把石油分成不同沸点范围的产品
B.硝酸工业中,为了加快氨氧化的速率,通常使用铁触媒作催化剂
C.纯碱工业中,氨碱法通过氨气和二氧化碳的循环利用,提高了原料的利用率
D.合成氨工业中,采用高压条件,增大合成氨反应的平衡常数,增大原料转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com