
下列有关铁及其化合物的说法中不正确的是( )
A.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
C.工业上可用铁质容器储存、运输浓硝酸和浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
有X、Y、Z三种单质,X为金属单质,Y、Z为非金属单质,Y、Z通常情况下为气态,Y、Z一定条件下反应的产物溶于水可得无色溶液E,E能使紫色石蕊试液变红,X与E反应可生成Z和另一产物w,X、Y反应的产物F溶于水为棕黄色溶液,将Y通入w溶液也可得到F的溶液。
(1)Z的化学式是 。 (2)w的名称是 。
(3)棕黄色溶液F中加入氨水的离子方程式是
(4)若往w溶液中滴入NaOH溶液,可产生沉淀,此沉淀在空气中发生变化的现象是___________; 方程式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关除杂的实验操作合理的是
A.除去二氧化碳中混有的少量一氧化碳:通入适量氧气后点燃
B.除去氧气中少量氮气:使气体通过炽热的铜粉
C.除去石英中少量碳酸钙:用稀盐酸溶解后过滤
D.除去氯化钠固体中少量的纯碱:加入足量氯化钙,过滤、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为____________________________________
_________________________________________________________________。
(2)混合①中使用冰水的目的是_______________________________________
_________________________________________________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是________、________。操作Ⅲ一般适用于分离________混合物。(选填编号)
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是__________________________________________
________________________________________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色,于是甲乙丙同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为_____ _________,若假设成立,可观察到的现象为________________________。乙同学假设工业氢溴酸呈淡黄色是因为________________,其用于证明该假设所用的试剂为________。
_________,若假设成立,可观察到的现象为________________________。乙同学假设工业氢溴酸呈淡黄色是因为________________,其用于证明该假设所用的试剂为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某酿造厂生产的“老谢琼醋”是一种优质琼醋。某高二年级研究性学习小组,运用酸碱中和滴定的原理对“老谢琼醋”进行了定量分析,以测定其中的酸(全部以醋酸CH3COOH计)的含量:用酸式滴定管取10.00 mL这种琼醋,置于已知质量的小烧杯中称得其质量为12.5 g,再用100 mL容量瓶稀释至100 mL,滴定时每次取20.00 mL于锥形瓶中,而选用的标准溶液是0.112 5 mol/L NaOH溶液,以及合适的指示剂。读取的数据记录如下,其中第3次滴定的读数请从下图中读取。
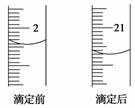
| 滴定次数 | 用去NaOH溶液的体积 | ||
| 滴定前刻度 | 滴定后刻度 | 体积(mL) | |
| 1 | 3.20 | 22.48 | |
| 2 | 1.23 | 20.55 | |
| 3 | — | — |
(1)请把有关数据填入表中所有空格里。
(2)琼醋样品从取出、称量、稀释到取液过程中,下列仪器水洗后不应再用相应琼醋润洗的仪器是________。
A.酸式滴定管 B.烧杯
C.100 mL容量瓶 D.锥形瓶
(3)滴定时在锥形瓶底垫一张白纸的作用___________________________________________。
(4)滴定操作时,左手应____________,观察滴定管里液面的高度时应注意________________________________。
(5)选用的合适指示剂是________,变色情况是____________________________________。
(6)计算稀释后容量瓶中醋酸的物质的量浓度________________________________________________。
(7)计算“老谢琼醋”中醋酸的质量分数________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的Fe和Fe2O3混合物投入2 mol/L250 mL的HNO3溶液中,反应完全后,无固体剩余,生成1.12 L NO气体(标准状况),再向反应后溶液中加入1 mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
A.450 mL B.500 mL
C.400 mL D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1 mol Ag。则下列结论中不正确的是( )
A.反应后溶液中Cu2+与Fe2+的物质的量之比为1∶2
B.氧化性:Ag+>Fe3+>Cu2+>Zn2+
C.含Fe3+的溶液可腐蚀铜板
D.1 mol Fe可还原3 mol Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质:①水 ②醋酸 ③盐酸 ④烧碱 ⑤硝酸钾 ⑥酒精 ⑦汽油 ⑧蔗糖
(用编号回答)其中属于弱电解质的有 ;属于强电解质的有 ;强电解质在水中 电离。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验过程中,始终无明显现象的是
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com