
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
| 16.02ml+16.00ml+16.01ml |
| 3 |
| 16.02ml+16.00ml+16.01ml |
| 3 |
| 0.2000g |
| 134g/mol |
| ||
| 0.01601L |
| ||
| 0.01601L |


科目:高中化学 来源: 题型:
| A、原子半径 Na<Mg<Al |
| B、热稳定性 HCl>H2S>PH3 |
| C、酸性强弱 H2SiO3<H2CO3<H3PO4 |
| D、熔点 NaCl>Na>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3 AgNO3 HNO3 |
| B、AgNO3 Na2CO3 HCl |
| C、AgNO3 Na2CO3 HNO3 |
| D、AgNO3 K2CO3 HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
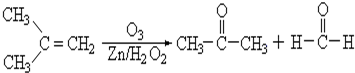
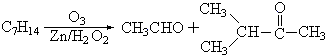
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(NO)=0.08mol/(L?s) |
| B、v(O2)=0.01mol/(L?s) |
| C、v(NH3)=0.002mol/(L?s) |
| D、v(H2O)=0.004mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁腐蚀时可能发生的正极反应:4OH--4e-→2H2O+O2↑ |
| B、明矾水解反应的离子方程式:Al3++3H2O→Al(OH)3+3H+ |
C、乙烯的结构式: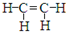 |
D、苯分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com