
| A、Ag+和Cl-在水溶液中混合,其反应的活化能接近于零 |
| B、活化能的大小对化学反应前后的能量变化能产生影响 |
| C、加催化剂能降低正反应的活化能,但不降低逆反应的活化能 |
| D、温度降低,反应速率减慢,其原因是降低了反应的活化能 |


科目:高中化学 来源: 题型:
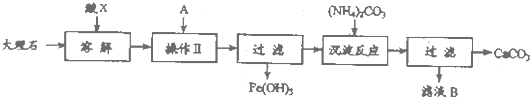
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | Q | R | X | Z | ||
| 微粒信息 | 离子: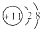 | 单质分子:R2 | 离子:X3+ | 一种原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、Q1=Q2=Q3 |
| B、Q2>Q3>Q1 |
| C、Q1>Q2>Q3 |
| D、Q1<Q2═Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2-丁炔与1,3-丁二烯稳定性的相对大小 |
| B、2-丁炔与1,3-丁二烯分子储存能量的相对高低 |
| C、2-丁炔与1,3-丁二烯相互转化的热效应 |
| D、一个碳碳叁键的键能与两个碳碳双键的键能之和的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、G点时沉淀的质量为18.5g |
| B、该混合溶液中6c(Fe3+)>c(NO3-) |
| C、该混合溶液在空气中加热、蒸干、灼烧后所得到的固体为Fe(NO3)3和Al(NO3)3 |
| D、室温下Ksp[Al(OH)3]>Ksp[Fe(OH)3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠的活泼性比铜的强,所以钠可和硫酸铜溶液反应生成铜 |
| B、氢氧化铝是两性氢氧化物,所以氢氧化铝可溶解在氨水中 |
| C、浓硝酸易分解,所以要用棕色瓶盛放,且放在阴凉处保存 |
| D、金刚石是自然界中硬度最大的物质,所以金刚石不能与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
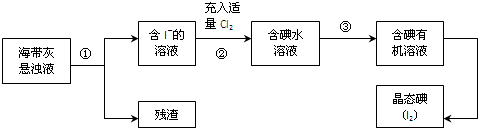
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4?5H2O属于纯净物 |
| B、凡能电离出H+的化合物均属于酸 |
| C、纯碱、烧碱、碱石灰均属于碱 |
| D、盐类物质一定含有金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com