
【题目】将下列各组物质按酸、碱、盐分类顺序排列,正确的是
A. 硫酸、纯碱、石膏 B. 氢硫酸、烧碱、绿矾
C. 碳酸、乙醇、醋酸钠 D. 磷酸、熟石灰、苛性钾
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】简答题:
(1)NH4Cl溶液呈 , 用离子方程式表示原因 .
(2)普通泡沫灭火器的钢铁容器里装着一只小玻璃筒,其中玻璃筒内盛装溶液,使用时,倒置灭火器,两种药液相混合就会喷出含二氧化碳的白色泡沫.产生此现象的离子方程式是 .
(3)NaHSO3溶液呈性,原因 .
(4)在25℃下,向浓度均为0.1molL﹣1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为 . 已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Cu(OH)2]=2.2×10﹣20 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法错误的是
A.生活中“卤水点豆腐”的原理是Mg2+、Ca2+等离子使蛋白质胶体发生聚沉
B.有机玻璃和高温结构陶瓷都属于新型无机非金属材料
C.新能源汽车的推广与使用有利于减少光化学烟雾的产生
D.茶叶中含有的茶多酚可用于制备食品防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用标准的0.2mol/L的盐酸滴定待测的NaOH溶液,其实验操作如下:A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2﹣3滴酚酞指示剂.
B.用待测的NaOH溶液润洗碱式滴定管.
C.检查滴定管是否漏水.
D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻度“0”以上2cm﹣3cm处,把酸式滴定管固定好,调节液面.
E.把滴定管用蒸镏水洗净,并分别固定在滴定管架两边.
F.另取锥形瓶,再重复滴定操作一次.
G.把锥形瓶放在酸式滴定管的下面,瓶下垫一张白纸,然后边滴定边摇动锥形瓶,直至终点,记下滴定管的液面所在刻度.
据上述滴定操作,完成下列填空:
(1)滴定操作的正确操作顺序是(用上述各编号字母填写)→E→→B→→→;
(2)G步操作中判断滴定终点的依据是;
(3)D步骤的操作中液面应调节到 , 尖嘴部分应;
(4)酸式滴定管未用标准的盐酸润洗,待测溶液NaOH的测定值会;碱式滴定管未用待测的NaOH溶液润洗,待测NaOH溶液的测定值会 . (填“偏高”、“偏低”或“无影响”.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,回答下列问题。
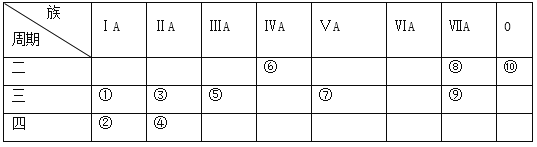
(1)这10种元素中,化学性质最不活泼的元素是____(写序号),得电子能力最强的原子是____(用元素符号表示);元素⑦的最高价氧化物对应的水化物是______(写化学式)。
(2)元素④的离子结构示意图为____________________________。
(3)①、⑧、⑨三种元素单核离子半径由大到小的顺序是(用离子符号表示)_____________。
(4)请写出:
(ⅰ)③的单质置换出⑥的单质的化学方程式:___________________________。
(ⅱ)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式:__________________。
(ⅲ)②和⑨两种元素最高价氧化物对应的水化物相互反应的离子方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的保存不正确的是
A. AgNO3溶液应保存在棕色瓶中 B. 浓硫酸要密封保存
C. 液氯可以保存在干燥的钢瓶中 D. 漂白粉露置于空气中保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知aAm+与bBn-具有相同的核外电子排布,则下列关系正确的是
A. a=b+m+n B. a=b-m+n C. a=b+m-n D. a=b-m-n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等固定装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.请填写下列空白: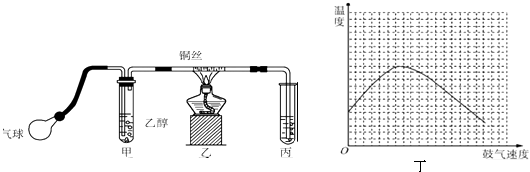
(1)检验乙醛的试剂是(填字母).
A.银氨溶液
B.碳酸氢钠溶液
C.新制Cu(OH)2
D.氧化铜
(2)乙醇发生催化氧化反应的化学方程式为: .
(3)实验时,常常将甲装置浸在70~80℃的水浴中,目的是 , 由于装置设计上的缺陷,实验进行时可能会 .
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图丁所示.试解释鼓气速度过快,反应体系温度反而下降的原因 , 该实验中“鼓气速度”这一变量你认为可用来估量.
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确? .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com