
【题目】(1)氮和碳的化合物与人类生产、生活密切相关。已知:
N2(g)+O2(g)===2NO(g);ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH= 。
(2)在压强为0.1 MPa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g);ΔH<0。
CH3OH(g);ΔH<0。
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增大甲醇产率的是 (填字母)。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)如图所示的装置能吸收和转化NO2和SO2。
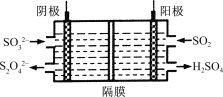
阳极区的电极反应式为 。
②阴极排出的溶液中含S2O![]() 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO![]() 可在阴极区再生。写出该反应的离子方程式: 。
可在阴极区再生。写出该反应的离子方程式: 。
(4)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
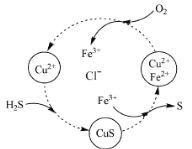
①在图示的转化中,化合价不变的元素是 。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为 。
【答案】
(1)-664.1kJ·mol-1(2)①c(CH3OH)/c(CO)·c2(H2)②B
(3)①SO2-2e-+2H2O===SO![]() +4H+②4S2O
+4H+②4S2O![]() +2NO2+8OH-=8SO
+2NO2+8OH-=8SO![]() +N2+4H2O
+N2+4H2O
(4)①铜、氢、氯②0.5mol
【解析】
试题分析:(1)①已知:①N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
②2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1,
依据盖斯定律可知②-①得:2H2(g)+2NO(g)=N2(g)+2H2O(l),
△H=(-483.6 kJ/mol)-180.5kJ/mol═-664.1 kJ/mol;
(2)①CO(g)+2H2(g)CH3OH(g)△H<0,反应的平衡常数为:K=![]() ;
;
②A.升高温度,平衡逆向进行,甲醇产率减小,故A错误;B.将CH3OH(g)从体系中分离,平衡正向进行,甲醇产率增大,故B正确;C.充入He,使体系总压强增大,分压不变,平衡不动,故C错误;故答案为B;
(3)①依据图示可知,二氧化硫在阳极区域被氧化为硫酸根,即阳极区发生反应SO2-2e-+2H2O═SO42-+4H+;②阴极排出的S2O![]() 离子,能将NO2气体转化为无污染气体,此气体为N2,同时生成SO
离子,能将NO2气体转化为无污染气体,此气体为N2,同时生成SO![]() ,根据电子守恒、电荷守恒及原子守恒可知该反应的离子方程式为4S2O
,根据电子守恒、电荷守恒及原子守恒可知该反应的离子方程式为4S2O![]() +2 NO2+8OH-=8SO
+2 NO2+8OH-=8SO![]() +N2+4H2O;
+N2+4H2O;
(4)①根据图中各元素化合价知,Cu元素化合价都是+2价、H元素化合价都是+1价、Cl元素化合价都是-1价,所以化合价不变的是Cu、H、Cl元素;②H2S不稳定,易被氧气氧化生成S单质,反应方程式为2H2S+O2=2S+2H2O,该反应中S元素化合价由-2价变为0价、O元素化合价由0价变为-2价,根据氧化还原反应中得失电子相等得,反应中当有1mol H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,消耗O2的物质的量=![]() =0.5mol。
=0.5mol。


科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子或分子在指定溶液中可能大量共存的是
A.pH=7的溶液:Fe3+、NH4+、Cl-、NO3-
B.水电离出的c(H+)=1.0×10-12mol·L-1的溶液中:Na+、SO42-、HCO3-、K+
C.由水电离出的c(OH-)=1.0×10-2mol·L-1的溶液:Cl-、CH3COO-、K+、[Al(OH)4]-
D.![]() =1012的溶液中,NH4+、Al3+、NO3-、Cl-
=1012的溶液中,NH4+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的两极分别为Pb和PbO2,电解质溶液为硫酸,工作时反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论正确的是( )
A. Pb为正极,发生氧化反应 B. 外电路电流由PbO2流向Pb
C. SO42-只向正极移动 D. 溶液的c(H+)不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理,按照如图所示装置连接,电解40min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30min,即可得到更加致密的氧化膜。下列有关说法正确的是

A.电解时,电子从电源负极→导线→铝极,铅极→导线→电源正极
B.在电解过程中,H+向铝片移动,SO42-向铅片移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+==2Al3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。下列叙述正确的是
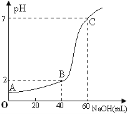
A.所用HCl的浓度是0.09mol·L─1,NaOH溶液浓度为0.03mol·L─1
B.在B点,溶液中离子浓度关系为:c(Cl─)>c(H+)>c(Na+)>c(OH─)
C.A、B、C三点由水的电离产生的c(H+)大小依次为:A>B>C
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据统计,金属腐蚀造成的损失远远超过火灾、水灾等自然灾害的总和,越来越被世界各国所重视,下面金属的防腐措施中,使用牺牲阳极的阴极保护法的是( )
A. 汽车底盘喷涂油漆 B. 地下钢管连接锌块
C. 钢闸门连接电源负极 D. 掺防腐的金属制成不锈钢菜刀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象预测正确的是
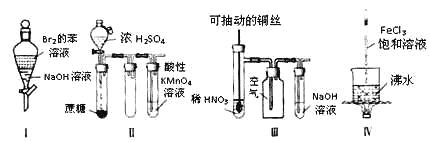
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:继续煮沸溶液至红褐色沉淀,停止加热,当光束通过体系时一定不可产生丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com