
【题目】下列实验现象预测正确的是
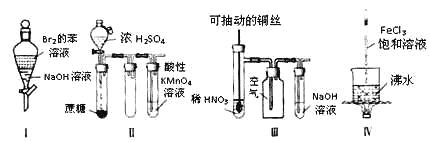
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:继续煮沸溶液至红褐色沉淀,停止加热,当光束通过体系时一定不可产生丁达尔效应
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】(1)氮和碳的化合物与人类生产、生活密切相关。已知:
N2(g)+O2(g)===2NO(g);ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH= 。
(2)在压强为0.1 MPa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g);ΔH<0。
CH3OH(g);ΔH<0。
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增大甲醇产率的是 (填字母)。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)如图所示的装置能吸收和转化NO2和SO2。
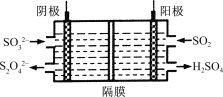
阳极区的电极反应式为 。
②阴极排出的溶液中含S2O![]() 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO![]() 可在阴极区再生。写出该反应的离子方程式: 。
可在阴极区再生。写出该反应的离子方程式: 。
(4)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
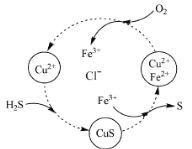
①在图示的转化中,化合价不变的元素是 。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是
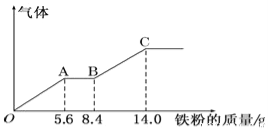
A.H2SO4浓度为2.5mol·L-1
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.原混合酸中NO3-的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的稀硫酸与足量的铝粉反应时,为了减缓反应速率,且不影响生成氢气的总量,应向稀硫酸中加入适量的
A.KOH(固体) B.CH3COOH C.KCl(固体) D.CH3COOK(固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,能证明醋酸是弱电解质的是
A. 水溶液的导电能力很弱 B. 溶液中已电离出的离子和未电离的分子共存
C. 能和氢氧化钠溶液反应 D. 熔化状态时不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,1 mol/L醋酸加水稀释至0.01 mol/L,关于稀释前后的下列变化正确的是
A.溶液中c(OH-)减小 B. pH的变化值等于2
C.溶液中![]() 的值增大 D. Kw的值减小
的值增大 D. Kw的值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.124gP4含有的P-P键数为4NA(设NA表示阿伏伽德罗常数的值)
B.Be和NaOH溶液反应的离子方程式是:2Be+2OH-+2H2O=2BeO2-+3H2↑
C.在NaCl溶液中加入AgNO3溶液,生成白色沉淀;在加入氨水,沉淀消失。沉淀消失发生的离子方程式是:AgCl+2NH3·H2O=[Ag(NH3)2]++Cl-+2H2O
D.0.1mol/L的Fe3+溶液中,能大量共存的离子有Cl-、SO42-SCN-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com