
����Ŀ���ڱ�״���£���224LHCl�����ܽ���635mLˮ�У�����������ܶ�Ϊ��1.18gcm��3���Լ��㣺
(1)����������������������ʵ���Ũ���Ƕ��٣�___��___
(2)ȡ����������100mL��ϡ����1.18L��������ϡ��������ʵ���Ũ�ȡ�___
(3)����������Na2CO3��NaOH��Ʒ2.53g������50.0mL2.00molL��1�������У���ַ�Ӧ�����ɱ�״���¶�����̼����112mL����Һ���ԣ��кͶ����������ȥ40.0mL1.00molL��1��NaOH��Һ�������кͺ����Һ�����յõ����ٿ˹��壿___
���𰸡�36.5% 11.8mol/L 1molL��1 5.85��
��������
(1)����n=![]() ����HCl���ʵ���������m=nM����HCl����������m=��V����ˮ������������������Һ��������������c=
����HCl���ʵ���������m=nM����HCl����������m=��V����ˮ������������������Һ��������������c=![]() ������Һ���ʵ���Ũ�ȣ�
������Һ���ʵ���Ũ�ȣ�
(2)����ϡ�Ͷ���c(Ũ)V(Ũ)=c(ϡ)V(ϡ)���㣻
(3)������Ӧ�������кͺ����Һ��������ù���ΪNaCl������ClԪ���غ㣺n(NaCl)=n(HCl)���ٸ���m=nM���㡣
(1)n(HCl)=![]() =10mol�� m(HCl)=10mol��36.5gmol1=365g��635mLˮ������Ϊ635mL��1g/mL=635g���������������
=10mol�� m(HCl)=10mol��36.5gmol1=365g��635mLˮ������Ϊ635mL��1g/mL=635g���������������![]() =
=![]() ��100%=36.5%��c(HCl)=
��100%=36.5%��c(HCl)= ![]() =
=![]() =11.8mol/L�������������������Ϊ36.5%�����ʵ���Ũ����11.8mol/L���𰸣�36.5% 11.8mol/L��
=11.8mol/L�������������������Ϊ36.5%�����ʵ���Ũ����11.8mol/L���𰸣�36.5% 11.8mol/L��
(2)����c(Ũ)V(Ũ)=c(ϡ)V(ϡ)����֪c(ϡ)=11.8molL1��0.1L��1.18L=1molL1��
����ϡ��������ʵ���Ũ��1molL1���𰸣�1molL1��
(3)������Ӧ�������кͺ����Һ��������ù���ΪNaCl������ClԪ���غ㣺n(NaCl)=n(HCl)=0.050L��2molL1=0.1mol��m(NaCl)=0.1mol��58.5gmol1=5.85g�����յõ�����5.85g�����Դ𰸣�5.85g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ��Ӧ�ñȽϹ㷺���Ķ�����IJ��ϣ������ػ�ѧ֪ʶ�ش��������⡣�ڻ�ҩ��Ҫ������ء���ǡ�ľ̿���߷�ĩ�Ļ����ڵ�ȼ�����£��仯ѧ��Ӧʽ��ҪΪ��2KNO3+S+3C=N2��+3CO2��+K2S
��1���ںڻ�ҩȼ�յķ�Ӧ�У�������Ϊ___��
��2���÷�Ӧ��������Ԫ����___��
��3���÷�Ӧ������������___��
��4��KNO3��NԪ�صĻ��ϼ���___��
��5�����ݻ�ѧ��Ӧʽ������һ����ԭ�Ӳ��뷴Ӧʱת��___�����ӣ�
��6����Cl2ͨ��Ũ��ˮ�У��������·�Ӧ��3Cl2+8NH3=6NH4Cl+N2����˫���ű�ʾ��Ӧ�ĵ���ת�Ʒ������Ŀ��___��
��7����֪�������з�Ӧ����ClO3-��5Cl-��6H+ =3Cl2��3H2O ��2Fe2+��Cl2=2Fe3+��2 Cl-����ClO3-��Fe3+��Cl2����������������ǿ������˳����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20mL0.1molL��1��H2A����Ԫ���ᣩ��Һ�еμ�0.1mol/L��NaOH��Һ����ҺpH��NaOH��Һ����ı仯��ͼ��ʾ������˵����ȷ����
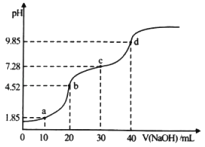
A.a�����Һ�У�c��Na+����c��A2����c��HA����c��H+����c��OH��
B.b�����Һ�У�c��H2A��+c��H+����c��A2��+c��OH��
C.c����Һ��pH��7������Ϊ��ʱHA�ĵ�������С����ˮ������
D.����0.1molL��1��NaOH��Һ����ͬŨ�ȵİ�ˮ�����μ�40mLʱ����ʱ��Һ��pH��9.85
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Ĺ�ҵ��ˮ�к��д�����FeSO4�ͽ϶��Cu2+��Ϊ�˼�����Ⱦ���Ϊ���������ƻ��Ӹ÷�ˮ�л������������ͽ���ͭ�����������ͼ����ͼ�����ش��������⡣

��1�������������õ�������____��
��2������A�ijɷ���___��____���������ƣ�����������____��
��3����μ�����Һa����Ҫ������____��
��4�����յ�ͭ���������Ʊ�������CuSO4��5H2O������ͭ��0.22mol/LH2SO4��Һ��Ϻ��ڼ��ȵ�����²���ͨ�������Ϳ����Ƶ�CuSO4��Ȼ�����õ���Һ������һϵ�в�������õ�������д������CuSO4�Ļ�ѧ����ʽ��___��
��5��ijͬѧ���ܶ�Ϊ1.84g/cm3����������Ϊ 98%��Ũ������500mL0.22mol/L��ϡ������Һ����Ҫ�ù��Ϊ___mL����Ͳ��ȡ___mL��Ũ���ᡣ
��6�����Ƹ���Һ�Ĺ����У����в���ʹ������õ���ҺŨ��ƫС����___(����ĸ)��
A��ϡ���ܶ�Ϊ1.84g/cm3����������Ϊ 98%��Ũ����ʱ����С�Ľ�������������Һ
B��������ˮϴ���ձ�����Ͳ��������������ϴ��Һע������ƿ��
C������ʱ�������µ�ת����ƿ���ְ�Һ����ʹ����ڿ̶��ߣ��ٲ���ˮ���̶���
D����ȡ�ܶ�Ϊ1.84g/cm3����������Ϊ 98%��Ũ����ʱ��������Ͳ�Ŀ̶���
E��ϴ������ƿ����������������Һ
F��ϡ��Ũ�����������������Һת�Ƶ�����ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
�غ͵����ػ������ڻ�����ҽҩ�����ϵ��������Ź㷺��Ӧ�á��ش��������⣺
��1��Ԫ��K����ɫ��Ӧ���Ϻ�ɫ��������ɫ��Ӧ�ķ��䲨��Ϊ_______nm�����ţ���
A��404.4 B��553.5 C��589.2 D��670.8 E.766.5
��2����̬Kԭ���У��������ռ�ݵ�����ܲ�ķ�����_________��ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ___________��K��Cr����ͬһ���ڣ��Һ����������ӹ�����ͬ��������K���۵㡢�е�ȶ��Ƚ���Cr�ͣ�ԭ����___________________________��
��3��X��������ⶨ�ȷ��֣�I3AsF6�д���I3+���ӡ�I3+���ӵļ��ι���Ϊ_____________������ԭ�ӵ��ӻ���ʽΪ________________��
��4��KIO3������һ���������õķ����Թ�ѧ���ϣ����и��ѿ��͵�����ṹ���߳�Ϊa=0.446nm��������K��I��O�ֱ��ڶ��ǡ����ġ�����λ�ã���ͼ��ʾ��K��O�����̾���Ϊ______nm����K���ڵ�O����Ϊ__________��
��5����KIO3�����ṹ����һ�ֱ�ʾ�У�I���ڸ�����λ�ã���K����______λ�ã�O����______λ�á�
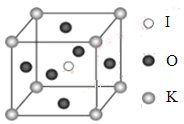
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪3CuO+2NH3![]() 3Cu+N2+3H2O�������ж���ȷ����
3Cu+N2+3H2O�������ж���ȷ����
A.NԪ�صĻ��ϼ۽���B.NH3����ԭ
C.����0.3 mol CuOת��0.6 NA������D.CuO�ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭ��CuCl)�㷺Ӧ���ڻ�����ӡȾ����Ƶ���ҵ��CuCl�����ڴ���ˮ��������������Ũ�Ƚϴ����ϵ���ڳ�ʪ��������ˮ���������Ժ���ͭ����Ҫ�ɷ���Cu������CuO��Ϊԭ�ϣ���������������ֽ⼼������CuCl�Ĺ��չ������£�
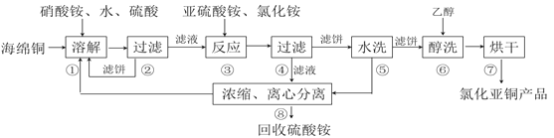
�ش��������⣺
��1���������еõ�������������_________���ܽ��¶�Ӧ������60~70�ȣ�ԭ����__________��
��2��д������������Ҫ��Ӧ�����ӷ���ʽ___________��
��3��������������pH=2����ϴ��ˮϴ������������ϴ���õ�����_________��д���ƣ���
��4�����������У�����������ʡ�ԣ�������______________________________��
��5����������������������Ҫ���й�Һ���롣��ҵ�ϳ��õĹ�Һ�����豸��__________������ĸ��
A�������� | B�����Ļ� | C����Ӧ�� | D����ʽѹ�˻� |
��6��ȷ��ȡ���Ʊ����Ȼ���ͭ��Ʒm g����������������FeCl3��Һ�У�����Ʒ��ȫ�ܽ��������ϡ���ᣬ��a mol/L��K2Cr2O7��Һ�ζ����յ㣬����K2Cr2O7��Һb mL����Ӧ��Cr2O72-����ԭΪCr3+����Ʒ��CuCl����������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����õ絼�ʴ������ɻ��Ƶ絼������ͼ����ͼΪ��0.1mol/LNaOH��Һ�ζ�10mL0.lmol/L��������еĵ絼�����ߡ�����˵���������

A. �絼�ʴ������������ж�����к͵ζ����յ�
B. a��b��c �����Һ�У�����Ũ���ɴ�С˳��Ϊa>b>c
C. d����ʾ��Һ�д��ڣ�c(Cl-) +c(OH-) =c(H+) +c(Na+)
D. C��絼����С����Ϊ��ʱ��Һ�е�������Ŀ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪pAg+=lgc(Ag+)��pX=lgc(X)��ij�¶��£�AgBr��AgCl��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������
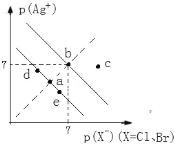
A. a��c�����Kw��ͬ
B. Ksp(AgCl)=1.0��1014 mol2��L2
C. ��AgCl��Һ�м���NaCl���壬��ʹa��䵽d��
D. AgCl(s)��Br(aq)![]() AgBr (s)��Cl(aq)ƽ�ⳣ��K=Ksp(AgCl)/Ksp(AgBr)
AgBr (s)��Cl(aq)ƽ�ⳣ��K=Ksp(AgCl)/Ksp(AgBr)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com