
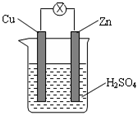
| A、锌片为负极,发生还原反应 |
| B、电流从锌片流向铜片 |
| C、一段时间后,铜片质量减轻 |
| D、一段时间后,溶液pH值变大 |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、潮湿疏松透气的土壤中 |
| B、含铁元素较多的酸性土壤中 |
| C、干燥致密不透气的土壤中 |
| D、含碳量较高,潮湿透气的中性土壤中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 甲烷 | 氨气 | 水 | 硫化氢 |
| 偶极矩(μ)/德拜尔 | 0 | 1.66 | 1.85 | 1.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
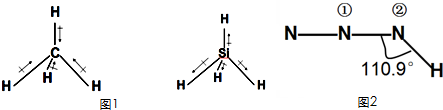
 意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知N-N键能167kJ?mol-1N≡N键能942kJ?mol-1.根据以上信息和数据,能判断且说法正确的是( )
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知N-N键能167kJ?mol-1N≡N键能942kJ?mol-1.根据以上信息和数据,能判断且说法正确的是( )| A、N4属于一种新型的化合物 |
| B、N4与N2互为同素异形体 |
| C、N4比P4(白磷)更稳定 |
| D、N4气体转变为N2将吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
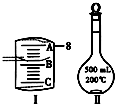 实验室要用Na2CO3?10H2O晶体配制500mL 0.1mol?L-1 Na2CO3溶液,回答下列问题:
实验室要用Na2CO3?10H2O晶体配制500mL 0.1mol?L-1 Na2CO3溶液,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com