
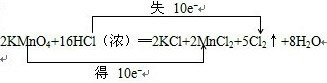 ,故答案为:
,故答案为: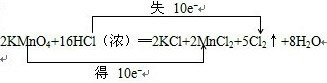 ;HCl.
;HCl.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、硫原子的原子结构示意图: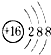 | ||
B、NH4Cl的电子式: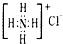 | ||
C、核内有8个中子的碳原子:
| ||
| D、HCO3-电离的离子方程式:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C、放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D、放电时的正极在充电时须接电源正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素铯的两种核素137Cs比133Cs多4个质子 |
| B、元素P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 |
| C、元素原子的最外层电子数越多,越容易得电子 |
| D、从上到下,第VIIA族元素氢化物的热稳定性和还原性均依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
88 22 |
A、一个
| ||
| B、Ra元素位于元素周期表中第六周期ⅡA族 | ||
| C、RaCl2难溶于水 | ||
| D、Ra(OH)2是一种两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 冰醋酸 | 福尔马林 | 苛性钾 | HI | 乙醇 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 胆矾 | 石灰水 | 硫酸钡 | HNO2 | NH3 |
| A、A、 | B、B、 | C、C、 | D、D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
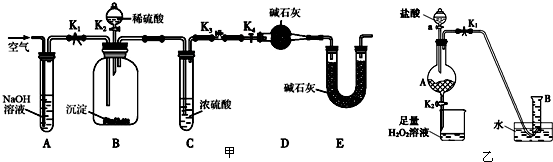
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com